
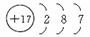
请回答下列问题:
(1)写出Z的原子结构示意图____________________________。
(2)写出图中D的电子式____________________________。
(3)确定图中单质F的依据是____________________________。
(4)利用图中反应③在标准状况下生成
(5)写出图中G溶液与H溶液相混合发生反应的离子方程式__________________________。
(6)如下图所示装置,两玻璃管中盛有A饱和溶液,两极为多孔石墨电极,给两极分别通入X2、Z2气体,电流表的指针发生偏转;通入X2气体的电极名称是_________________(填写“正极”或“负极”);通入Z2气体的电极反应式为____________________________。
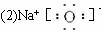
解析:依据X、Y、Z的原子序数关系和周期表相对位置关系,以及XZ、YZ形成化合物的比例(1∶1)和化合物类型可以知道X、Y分别为非金属和金属元素且为ⅠA族元素,所以X、Y、Z为H、Na、Cl。A为NaCl、E为HCl。代入框图推得B为H2、C为Cl2、D为NaOH。又单质F既可以和HCl反应,又可以和NaOH反应,所以在短周期内为Al。
(6)根据H2和Cl2的反应分析H2发生氧化反应、Cl2发生还原反应,结合原电池工作原理(负极发生氧化反应、正极发生还原反应)判断正负极,写出正极反应式。
答案:
(1)![]()
![]()
(3)初步判断E为盐酸,D为氢氧化钠,既与盐酸反应又与NaOH溶液反应的单质是金属铝
(4)1
(5)3AlO-2+Al3++6H2O![]() 4Al(OH)3↓
4Al(OH)3↓
(6)负极 Cl2+2e-![]() 2Cl-
2Cl-


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:

(1)写出元素符号:X___________,Y___________,Z___________。
(2)写出①②④的离子反应方程式。
①__________________________________________________________。
②__________________________________________________________。
④__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:

请回答下列问题:
(1)写出Z的原子结构示意图_______________。
(2)写出图中D的电子式_______________。
(3)确定图中单质F的依据是_______________。
(4)利用图中反应③在标准状况下生成
(5)写出图中G溶液与H溶液相混合发生反应的离子方程式_______________。
(6)如下图所示装置,两玻璃管中盛有A饱和溶液,两极为多孔石墨电极,给两极分别通入X2、Z2气体,电流表的指针发生偏转;通入X2气体的电极名称是_______________(填写“正极”或“负极”);通入Z2气体的电极反应式为_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
(22分)已知X、Y、Z三种短周期主族元素在元素周期表中的位置关系如图所示。
| Z |
|
| Y | X |
请回答:(1)三种元素中原子半径最大的是 (填X、Y或Z)
(2)若X的单质是黄绿色气体,则X和Y的最高价氧化物对应的水化物的酸性强弱顺序为 (用化学式表示),和X同主族元素氢化物中熔沸点最高的是 (用化学式表示),原因是 ;X单质溶于水生成物之一具有漂白性,写出该物质结构式 。
(3)若X的单质与强酸、强碱溶液反应均能放出氢气,则元素X在周期表中的位置 写出X单质和烧碱溶液反应的离子方程式
探究X和Y两种元素金属性强弱的实验方法是 。
(4)若Y的氧化物是制造光导纤维的材料,则Y元素的名称是 ,
工业上利用单质Z和Y的氧化物高温下反应,生成一种具有空间立体网状结构的化合物,另一种生成物是有毒气体,写出反应化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年福建省福州八县(市)一中高二下学期期中联考化学试卷 题型:填空题
(22分)已知X、Y、Z三种短周期主族元素在元素周期表中的位置关系如图所示。
| Z | |
| Y | X |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com