
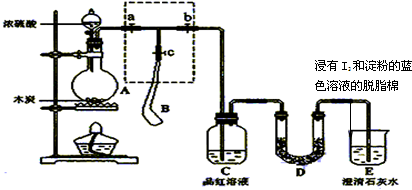
分析 (1)浓硫酸有强氧化性,能将C氧化为二氧化碳;碘单质能将二氧化硫氧化为硫酸;
(2)设法使装置内外形成气压差是气密性检查的常用手段,根据气压差产生的现象判断气密性;
(3)为控制反应的速率,可先使气体充满B,用B中气体进行试验;
(4)二氧化硫能使品红溶液褪色;
(5)D装置用碘与二氧化硫反应除去二氧化硫,所以在进气一端碘与二氧化硫反应使得进气口一端脱脂棉蓝色变浅,在出气口一端二氧化硫被除尽,出气口一端脱脂棉蓝色不变,说明出气口出的是二氧化碳;
(6)根据(5)的分析可知,装置D的作用为除去SO2并检验SO2已被除净;
解答 解:(1)装置A中浓硫酸有强氧化性,能将C氧化为二氧化碳,反应方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,D中碘单质能将二氧化硫氧化为硫酸,反应方程式为I2+SO2+2H2O=H2SO4+2HI,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;I2+SO2+2H2O=H2SO4+2HI;
(2)设法使装置内外形成气压差,采取的操作是关闭分液漏斗的活塞,打开止水夹a和b,关闭止水夹c,用手捂热(或微热)圆底烧瓶A,若C中有气泡冒出,移开手掌(或热源)后,C处导管内有水上升,则证明A装置的气密性良好,
故答案为:关闭分液漏斗的活塞,打开止水夹a和b,关闭止水夹c,用手捂热(或微热)圆底烧瓶A,若C中有气泡冒出,移开手掌(或热源)后,C处导管内有水上升,则证明A装置的气密性良好;
(3)为控制反应的速率,先用气囊将气体收集起来,再用气囊中气体进行试验,所以操作为:打开止水夹a和c,关闭止水夹b;向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b,故答案为:③①②;
(4)二氧化硫能使品红溶液褪色,故答案为:品红溶液褪色;
(5)D装置用碘与二氧化硫反应除去二氧化硫,所以在进气一端碘与二氧化硫反应使得进气口一端脱脂棉蓝色变浅,在出气口一端二氧化硫被除尽,出气口一端脱脂棉蓝色不变,说明出气口出的是二氧化碳,
故答案为:进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变;
(6)根据(5)的分析可知,装置D的作用为除去SO2并检验SO2已被除净,
故答案为:除去SO2并检验SO2已被除净.
点评 本题考查浓硫酸的性质、二氧化硫的性质,注意掌握实验的步骤和实验中装置的作用来解答,难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| B. | 小苏打用于治疗胃溃疡病人的胃酸过多症 | |
| C. | 计算机芯片所用的材料是高纯度的硅 | |
| D. | 纯净的二氧化硅是生产光纤制品的基本原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ①③④⑤ | C. | ③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
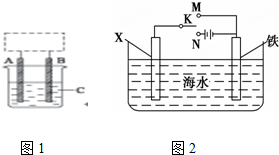 (I)研究CO2的利用对促进低碳社会的构建具有重要的意义.将CO2与焦炭作用生成CO,CO可用于炼铁等.
(I)研究CO2的利用对促进低碳社会的构建具有重要的意义.将CO2与焦炭作用生成CO,CO可用于炼铁等.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4g | B. | 3.6g | C. | 4.8g | D. | 6.0g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com