
| A. | 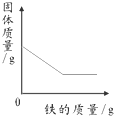 | B. | 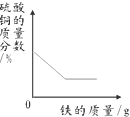 | C. | 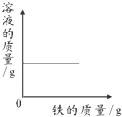 | D. | 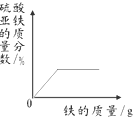 |
分析 由Fe+CuSO4=Cu+FeSO4可知,每反应56份的铁则会生成64份的铜,所以随着反应的进行固体质量在不断增加,而硫酸铜的质量会不断变小,硫酸亚铁的质量会不断变大,以此来解答.
解答 解:A.铁能与硫酸铜反应生成铜和硫酸亚铁,由于每反应56份的铁则会生成64份的铜,所以固体的质量会不断增大直至反应结束,图象不符,故A错误;
B.随着反应的进行,溶液中硫酸铜的质量逐渐减小,其溶质质量分数逐渐减小,最终硫酸铜反应耗尽,其溶质质量分数变为零,图象不符,故B错误;
C.由Fe+CuSO4=Cu+FeSO4可知,每160份质量的硫酸铜反应可得152份质量的硫酸亚铁,所以随着反应的进行溶液质量会不断变小,直至反应结束,图象不符,故C错误;
D.随着反应的进行,溶液中硫酸亚铁的质量从零逐渐增大,其溶质质量分数逐渐增大,直至反应结束其溶质质量分数不再变化,图象符合,故D正确;
故选D.
点评 本题考查金属及活泼性的应用,为高频考点,把握金属的置换反应及各物质的质量关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
 为测定某含铝镁合金(不含其它元素)中镁的质量分数,研究性学习小组的三位同学,设计下列三种不同实验方案进行探究.填写下列空白:
为测定某含铝镁合金(不含其它元素)中镁的质量分数,研究性学习小组的三位同学,设计下列三种不同实验方案进行探究.填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 变化过程中化学键被破坏,则一定发生化学变化 | |
| B. | 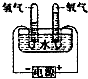 实验室制氧气 | |
| C. | Na+、Fe3+-人体所需微量元素 | |
| D. | 能区别地沟油与矿物油的方法是加入足量氢氧化钠溶液共热,不分层的是地沟油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它是一种含氮的有机化合物 | |
| B. | 它的相对分子质量为126g/mol | |
| C. | 它易溶于苯、四氯化碳等有机溶剂 | |
| D. | 由于它的含氮量高,被不法商人添加到奶粉中,以提升奶粉检测中的蛋白质含量指标 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
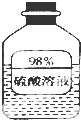 (1)如图信息,瓶中溶液长期放置后溶质质量分数变小,是因为该物质具有吸水性.
(1)如图信息,瓶中溶液长期放置后溶质质量分数变小,是因为该物质具有吸水性.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用燃着的木条伸入集气瓶中检验二氧化碳 | |
| B. | 用水区分氢氧化钠固体和氯化钠固体 | |
| C. | 用铁粉除去FeSO4溶液中混有的CuSO4 | |
| D. | 用石灰水除去NaOH溶液中混有的Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数为NA的CO和N2的混合气体体积为22.4L,平均相对分子质量为28 | |
| B. | 体积不变的容器中进行的反应N2+3H2$?_{高温高压}^{催化剂}$2NH3,随着反应的进行气体密度逐渐减小 | |
| C. | Na2O2和NH4Cl浓溶液反应得到混合气体的平均相对分子质量可能是34 | |
| D. | 对于反应I2(g)+H2(g)$\stackrel{△}{?}$2HI(g)而言,达到平衡后,气体的平均相对分子质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
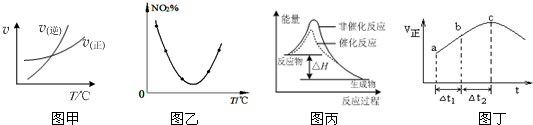
| A. | 由图甲表示的反应速率随温度变化的关系可知该反应的△H>0 | |
| B. | 图乙表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)═N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 | |
| C. | 图丙表示该反应为放热反应,且催化剂能改变反应的焓变 | |
| D. | 绝热恒容密闭容器中发生反应:SO2(g)+NO2(g)?SO3(g)+NO(g),其正反应速率随时间变化如图丁所示,则c点一定是平衡点 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com