
| 19.2g |
| 64g/mol |
| 0.8mol |
| 0.5L |


 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
| 5 |
| 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高纯度的硅单质广泛用于制作光导纤维 |
| B、传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料 |
| C、二氧化硅是制造玻璃的主要原料 |
| D、自然界中硅元素贮量丰富 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、MnO4-、Na+、Cl- |
| B、K+、Ba2+、NO3-、SO42- |
| C、Na+、Zn2+、NO3-、SO42- |
| D、H+、Na+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
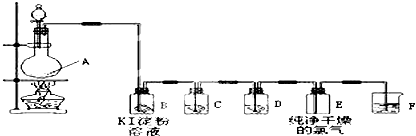
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、NO3-、MnO4- |
| B、K+、Na+、Br-、CH3COO |
| C、Mg2+、Na+、Cl-、SO42-- |
| D、Na+、Ba2+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将水加热,Kw增大,pH不变 |
| B、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| C、向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| D、向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 结构.分子中的四个磷原子位于正四面体的四个顶点.则P4分子中共有
结构.分子中的四个磷原子位于正四面体的四个顶点.则P4分子中共有
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com