
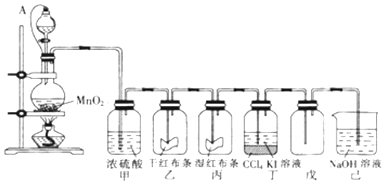
分析 (1)依据氯气不具有漂白性,次氯酸具有漂白性解答;
(2)氯气与碘化钾反应生成碘单质,碘易溶于四氯化碳,四氯化碳不溶于水,密度大于水;
(3)根据针头的作用判断压强的大小,气体的压强有利于分液漏斗内的液体顺利流下;
(4)二氧化锰和浓盐酸在加热条件下反应生成氯气、氯化锰和水;浓盐酸与MnO2发生化学反应,随着反应的进行,盐酸的浓度降低,还原性减弱,稀盐酸与MnO2不反应,以此解答该题;
(5)设二价铁离子物质的量为x,三价铁离子的物质的量为y,依据n(Fe元素):n(Cl元素)=1:2据此计算.
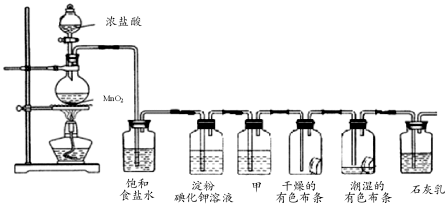
解答 解:(1)氯气不具有漂白性,次氯酸具有漂白性,通入到乙中的氯气为干燥氯气,所以不能使红色布条褪色,通入丙中的氯气与湿润布条中的水反应生成据有漂白性的次氯酸,所以有色布条褪色;
故答案为:干燥的红布条不褪色; 湿润的红布条褪色;
(2)氯气与碘化钾反应生成碘单质,碘易溶于四氯化碳,四氯化碳不溶于水,密度大于水,溶于分层,所以可以用分液的方法分离;
故答案为:分液;
(3)利用针头的橡皮管连接后,分液漏斗与烧瓶内气压相等,有利于液体流下;
故答案为:有利于球形分液漏斗里浓盐酸顺利流入烧瓶里;
(4)二氧化锰和浓盐酸在加热条件下反应生成氯气、氯化锰和水,化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
①n(HCl)=$\frac{146g}{36.5g/mol}$=4mol,浓盐酸与MnO2发生化学反应,随着反应的进行,盐酸的浓度降低,还原性减弱,稀盐酸与MnO2不反应,
∵4HCl(浓)→Cl2
∴生成的n(Cl2)<1mol;
②n(MnO2)=$\frac{87g}{87g/mol}$=1mol,由于浓盐酸足量,
∵MnO2→Cl2
∴生成的n(Cl2)=1mol,所以所得C12②比①多,
故答案为:A
(5)设二价铁离子物质的量为x,三价铁离子的物质的量为y,则氯离子的物质的量为2x+3y,依据n(Fe元素):n(Cl元素)=1:2.4可知:(x+y):(2x+3y)=1:2.4,解得x:y=3:2,
故答案为:3:2.
点评 本题考查了氯气的制取、性质,明确氯气制备原理及氯气、次氯酸的性质是解题关键,题目难度不大.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:选择题
| A. | 体积不变,向其中加入1mol H2 | |
| B. | 体积不变,向其中加入1mol N2 | |
| C. | 压强不变,向其中加入1mol N2 | |
| D. | 压强不变,向其中加入1mol H2和1molI2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
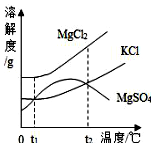 海洋资源开发前景十分广阔.海水晒盐能够得到粗盐和卤水,卤水中含有MgCl2、KCl和MgSO4等物质,图是它们的溶解度曲线.则下列说法不正确的是( )
海洋资源开发前景十分广阔.海水晒盐能够得到粗盐和卤水,卤水中含有MgCl2、KCl和MgSO4等物质,图是它们的溶解度曲线.则下列说法不正确的是( )| A. | t1℃时,三种物质的饱和溶液中,溶质质量分数最大的是MgCl2 | |
| B. | t1℃时,分别在100g水中溶解了等质量的MgCl2、KCl,两溶液都可达到饱和 | |
| C. | t2℃时,KCl和MgSO4两种物质的溶解度相同 | |
| D. | 将卤水加热到t2℃以上,析出的晶体主要为MgSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 油脂和蛋白质都属于高分子化合物 | |
| C. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| D. | 医用消毒酒精中乙醇的浓度为95% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
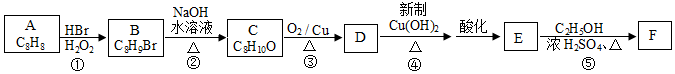
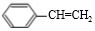 .
.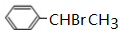 .
.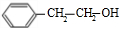 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2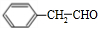 +2H2O、
+2H2O、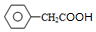 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$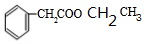 +H2O.
+H2O.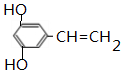 .
.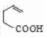 制备
制备 的合成路线.
的合成路线.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ①③ | C. | ⑤⑥ | D. | ⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 物质 | 起始浓度/(mol•L-1) | 平衡浓度/(mol•L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.0142 |
| NO2 | 0.100 | 0.0716 |
| A. | 平衡时,Ⅰ、Ⅱ中反应的转化率α(N2O4)>α(NO2) | |
| B. | 平衡后,升高相同温度,以N2O4表示的反应速率v(Ⅰ)<v(Ⅱ) | |
| C. | 平衡时,Ⅰ、Ⅱ中正反应的平衡常数K(Ⅰ)=$\frac{Ⅰ}{K(Ⅱ)}$ | |
| D. | 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 结论 | 原因 |
| A | 将氯气通入H2O2和NaOH的混合溶液中,导管口处发出红光,产生大量的气泡 | 该反应是放热反应,H2O2显示氧化性 |
| B | ZnS能溶解在稀盐酸中,CuS不能溶解在稀盐酸中 | CuS的Ksp比ZnS的Ksp小 |
| C | 在BaCl2和氨水混合溶液中通入CO2,有白色沉淀生成 | NH3在反应中作催化剂 |
| D | 单质硅不溶于浓硫酸和浓硝酸 | 硅被强氧化性酸钝化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com