
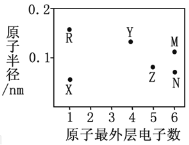
【题目】X、Y、Z、R、M、N为六种短周期元素,其原子半径和最外层电子数之间的关系如图所示。
(1)M元素的原子核外有__________种能量不同的电子,有__________个未成对电子;Z元素在元素周期表中的位置是第______周期________族。
(2)N、R、X三种元素的原子可构成一种强碱性物质,该物质的电子式是___________;Y元素的氧化物是制造光纤的主要材料,该氧化物是________晶体(填晶体类型)。某化工生产的核心环节的反应为:2MN2(g) + N2(g) 2 MN3(g) + Q(Q>0)
(3)该反应的平衡常数表达式![]() __________________________;欲使K值变大,可采取的措施是__________________________。
__________________________;欲使K值变大,可采取的措施是__________________________。
(4)该反应达到平衡后,在其他条件不变的情况下,若使得容器的体积扩大为原来的两倍,则平衡____________________。(选填“正向移动”、“逆向移动”或“不移动”)
【答案】52二ⅤA![]() 原子
原子![]() 或
或![]() 降温逆向移动
降温逆向移动
【解析】
X、Y、Z、R、M、N为六种短周期元素,X、R最外层只有一个电子,为第IA族元素;Y最外层有4个电子,位于第IVA族,Z原子最外层有5个电子,位于第VA族,M、N最外层有6个电子,位于第VIA族;R原子半径最大,为Na元素,X原子半径最小,为H元素;Y原子和Z原子半径接近、M原子半径大于Y而最外层电子数大于Y,所以Y是C、Z是N、N原子半径小于M ,则M为S元素、N为O元素;
(1)M为S元素,为16号元素,电子排布式为1s22s22p63s23p4,原子核外有5种能量不同的电子,有2个未成对电子;Z为N元素,在元素周期表中的位置是第二周期ⅤA族;
(2)N、R、X三种元素的原子可构成一种强碱性物质NaOH,该物质的电子式是![]() ;Y元素的氧化物SiO2是制造光纤的主要材料,该氧化物是原子晶体;
;Y元素的氧化物SiO2是制造光纤的主要材料,该氧化物是原子晶体;
(3)反应2MN2(g) + N2(g) 2 MN3(g)的平衡常数表达式![]() ;反应2MN2(g) + N2(g) 2 MN3(g) + Q(Q>0)为放热反应,降低温度平衡正向移动,K值增大,则欲使K值变大,可采取的措施是降温;
;反应2MN2(g) + N2(g) 2 MN3(g) + Q(Q>0)为放热反应,降低温度平衡正向移动,K值增大,则欲使K值变大,可采取的措施是降温;
(4)该反应达到平衡后,在其他条件不变的情况下,若使得容器的体积扩大为原来的两倍,压强减小,则平衡向气体体积增大的逆向移动。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极 a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8)。下列说法错误的是( )

A. 电池工作时,正极可发生反应:2Li2S6+2Li++2e-=3Li2S4
B. 电池工作时,外电路中流过 0.02 mol 电子,负极材料减重 0.14 g
C. 石墨烯的作用主要是提高电极a的导电性
D. 电池充电时间越长,电池中Li2S2的量越多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“生物质能”主要是指树木、庄稼、草类等植物直接或间接提供的能量,下列说法不正确的是
A. 生物质能是可储存和可运输的非可再生能源 B. 生物质能和化石燃料一样属于一次能源
C. 生物质能是解决农村能源的主要途径 D. 利用生物质能就是间接利用太阳能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g)![]() 2C(g)+Q达到平衡,下列说法正确的是
2C(g)+Q达到平衡,下列说法正确的是
A. 加压,v(正)、v(逆)都增大,增大倍数v(正)小于v(逆)
B. 降温,v(正)、v(逆)都减小,减小倍数v(正)小于v(逆)
C. 使用催化剂,v(正)、v(逆)都改变,变化的倍数不同
D. 扩大容器体积,容器内A、B、C物质的量都减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应:aX(g)+bY(g)![]() cZ(g)达到平衡时测得平衡常数为K1;保持温度不 变,将容器体积减小一半,当达到新平衡后,测得Y的浓度为原来的1.6倍,平衡常数为K2,则
cZ(g)达到平衡时测得平衡常数为K1;保持温度不 变,将容器体积减小一半,当达到新平衡后,测得Y的浓度为原来的1.6倍,平衡常数为K2,则
A. 平衡向正反应方向移动,K2>K1
B. 新平衡时Y的浓度增大,平衡向逆反应方向移动K1>K2
C. 新平衡时,Z的浓度大于原平衡2倍,K1=K2
D. 反应过程中,化学反应速率同等程度增大,K1=K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是关于有机物A、B、C的信息:
A | B | C |
①它的产量可衡量一个国家石油化工发展水平; ②能使溴的四氯化碳溶液褪色; ③可用于果实催熟. | ①C、H两种元素组成 ②分子球棍模型为 | ①分子键线式为 ②相对分子质量为68 |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为_______________;
(2)A在一定条件下,与水反应制乙醇的化学方程式:____________________;反应类型是______。
(3)B具有的性质是_____________________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤任何条件下均不与氢气反应
⑥一定条件下,能与CH2=CH2反应制苯乙烷 ⑦与溴水混合后液体分层且上层呈橙红色
(4)写出B的最简单同系物制TNT的化学方程式 _____________________;反应类型是________。
(5)C是天然橡胶的单体,写出天然高分子橡胶的结构简式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O===SO42-+2Fe 2++4H+;
②Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++7H2O。
下列有关说法不正确的是( )
A. SO2发生氧化反应
B. 若有13.44 L SO2(标准状况)参加反应,则最终消耗0.4mol K2Cr2O7
C. 氧化性:SO42- < Fe3+ < Cr2O72-
D. 每0.2 mol K2Cr2O7参加反应,转移电子的数目为1.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 在标准状况下,11.2L O2和22.4L NO混合并充分反应后得到的气体的分子数为NA
B. 常温下0.1mol·L-1NH4NO3溶液中的氮原子数为0.2NA
C. 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA
D. 25℃时,1.0L pH=13的Ba(OH)2溶液中,含有的OH-数目为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com