
已知热化学方程式:SO2(g)+ 1/2O2(g) 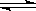 SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
A. 196.64kJ B. 小于196.64kJ C. 小于98.32kJ D.大于196.64kJ
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
聚乙炔衍生物分子M的结构简式及M在稀硫酸作用下的水解反应如图所示。下列有关说法不正确的是 ( )
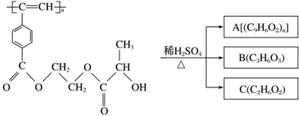
M
A.M与A均能使酸性高锰酸钾溶液和溴水褪色
B.B中含有羧基和羟基两种官能团,能发生消去反应和酯化反应
C.1 mol M与热的烧碱溶液反应,可消耗2n mol NaOH
D.A、B、C各1 mol分别与金属钠反应,放出气体的物质的量之比为1∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
C(s) + H2O(g) == CO(g) + H2(g);△H = +131.3 KJ/mol。它表示
A.碳与水反应吸收131.3 KJ的热量
B.固态碳和气态水各1mol反应,放出131.3 KJ的热量
C.1mol碳和1mol水反应吸收131.3 KJ的热量
D.1mol固态焦炭与1mol水蒸气反应产生一氧化碳和氢气,吸收131.3 KJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制硫酸接触室中生成SO3 的反应:2SO2(g)+ O2(g) 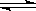 2SO3(g) △H<0,该反应的条件选择如下,其中可以完全用勒夏特列原理解释的是
2SO3(g) △H<0,该反应的条件选择如下,其中可以完全用勒夏特列原理解释的是
A 氧气过量 B使用催化剂
C 400 ℃~500℃的高温 D常压
查看答案和解析>>
科目:高中化学 来源: 题型:
在400 ℃、101 kPa时,NO2(g)+CO(g) = NO(g) + CO2(g) 反应过程的能量变化如下图所示。
|
|
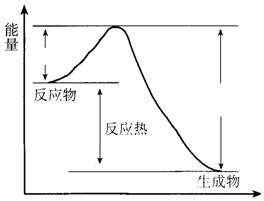
反应过程
(1)该反应是 (填“吸热”或“放热”)反应。
(2)该反应的热化学方程式为
。
(3)改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是 。
a.浓度 b.压强 c.温度 d.催化剂
(4)反应体系中加入催化剂对反应热是否有影响?_________(填“是”或“否”) ,
原因是______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关自发反应的说法中,正确的是
| A.自发反应都是放热反应 | B.自发反应都是熵增大的反应 |
| C.自发反应一定能发生 | D.非自发反应在一定条件下能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
 N2(g)+3H2(g)
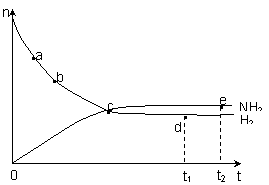
N2(g)+3H2(g) 2NH3(g) △H<0 , 673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
2NH3(g) △H<0 , 673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
A.点a的正反应速率比点b的小
B.点 c处反应达到平衡
C.点d (t1时刻) 和点 e (t2时刻) 处
n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,
n(H2)比上图中d点的值大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com