
科目:高中化学 来源: 题型:选择题
| A. |  称量 | B. | 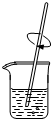 溶解 | C. |  蒸发 | D. | 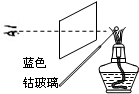 焰色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn+H2SO4═ZnSO4+H2↑ | B. | CaCO3+2HNO3═Ca(NO3)2+CO2↑+H2O | ||
| C. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | D. | BaCl2+Na2SO4═2NaCl+BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol/L MgCl2溶液中含Cl-数为2NA | |
| B. | 标准状况下,2.24 L 18O2中所含中子的数目是2NA | |
| C. | 1 mol Al3+含有核外电子数为10NA | |
| D. | 常温常压下,16 g CH4中含有的原子总数为5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 分子式 | 溶度积Ksp | 沉淀完全时的pH | 氯化钴晶体的性质 |
| Co(OH)2 | 5.9×10-15 | 9.4 | CoCl2•6H2O呈红色,常温下稳定.110~120℃时脱水变成蓝色无水氯化钴 |
| Fe(OH)2 | 1.6×10-14 | 9.6 | |
| Fe(OH)3 | 1.1×10-36 | 3.7 |
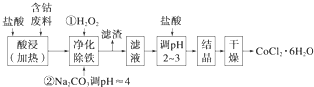
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硝酸钠不稳定,常温下即会分解,可用作食品添加剂 | |
| B. | 纸层析实验中,滤纸作为惰性支持物,展开剂作为流动相 | |
| C. | 牙膏中的安息香酸钠、氟化钠等溶于水,水解使溶液显酸性 | |
| D. | 欲分离硝酸钾和氯化钠的混合物(物质的量比为1:1),先将样品溶解,然后加热至表面出现晶膜后冷却,过滤得硝酸钾晶体;将母液加热至大量晶体析出后,用余热蒸干,得氯化钠晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
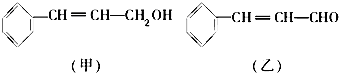
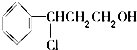 $\stackrel{O_{2}/Cu}{→}$Y$→_{Ⅱ}^{一定条件}$乙,其中反应Ⅰ的反应类型为加成反应,反应Ⅱ的化学方程式为
$\stackrel{O_{2}/Cu}{→}$Y$→_{Ⅱ}^{一定条件}$乙,其中反应Ⅰ的反应类型为加成反应,反应Ⅱ的化学方程式为 (注明反应条件).
(注明反应条件).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com