
 MnCl2 + Cl2↑ + 2H2O。
MnCl2 + Cl2↑ + 2H2O。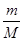 可知,8.7二氧化锰的物质的量=8.7g÷87g/mol=0.1mol
可知,8.7二氧化锰的物质的量=8.7g÷87g/mol=0.1mol MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O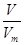 可知,生成的氯气在标准状况下的体积V=0.1mol×22.4L/mol=2.24L
可知,生成的氯气在标准状况下的体积V=0.1mol×22.4L/mol=2.24L

 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源:不详 题型:单选题
| A.2 mol | B.1 mol | C.0.5 mol | D.0.25 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:2 | B.2:1 | C.1:3 | D.3:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1∶2 | B.2∶1 | C.1∶3 | D.3∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是
与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是| A.反应中硫酸作氧化剂 | B. 中硫元素被氧化 中硫元素被氧化 |
| C.刺激性气味的气体是氨气 | D.1mol 完全反应转移0.5mol电子 完全反应转移0.5mol电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若用标准状况下4.48LCH4还原NO2生成N2和水蒸气,放出热量为173.4 kJ/mol |
| B.由反应①可推知CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l)△H﹥-574kJ/mol |
| C.反应②中当4.48LCH4反应完全时转移的电子总数为1.60mol |
| D.反应①②转移的电子数相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.M | B.M2+ | C.M3+ | D.MO2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com