
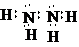 ,双氧水为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为:
,双氧水为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为: ,故答案为:
,故答案为: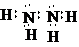 ;
; ;
;

科目:高中化学 来源: 题型:

| H2O/H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 重晶石(主要成分BaSO4)是制取可溶性钡盐的重要原料,工业上可用重晶石、焦炭、空气煅烧可制取BaS,其主要反应的热化学方程式如下:
重晶石(主要成分BaSO4)是制取可溶性钡盐的重要原料,工业上可用重晶石、焦炭、空气煅烧可制取BaS,其主要反应的热化学方程式如下:查看答案和解析>>
科目:高中化学 来源: 题型:
| t(℃) | 200 | 400 | 600 | 800 |
| ρ(g/L) | 6.881 | 4.236 | 2.650 | 1.517 |
| 气体摩尔体积(L/mol) | 38.8 | 55.2 | 71.6 | 88.0 |
| A、AlCl3 |
| B、Al2Cl6 |
| C、AlCl3和Al2Cl6 |
| D、Al3Cl9和Al2Cl6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、H+、NO3-、HCO3- |
| B、K+、Al(OH)4-、SO42-、NH3?H2O |
| C、Na+、K+、SO32-、ClO- |
| D、Na+、CH3COO-、SO42-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作 | 现象 | 结论 | |
| A | 向某无色溶液中滴加氯水和CCl4,振荡,静置 | 下层溶液显紫色 | 原溶液中有I- |
| B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3?H2O能大量共存 |
| C | 将铜片放入浓硝酸中 | 产生大量红棕色气体,溶液变为蓝绿色 | 浓硝酸有强氧化性和酸性 |
| D | 向Na2SiO3溶液中滴加酚酞,然后逐滴加入稀盐酸至红色退去 | 2min后,试管里出现凝胶 | 酸性:硅酸>盐酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3-CH=CH2分子中所有原子一定处于同一平面 |
| B、除去乙烷中的乙烯是将混气通入酸性KMnO4溶液中 |
| C、若烃中碳、氢元素的质量分数相同,它们可能是同系物 |
| D、某烷烃的命名为3,4,4一三甲基己烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com