
 HCl
HCl .
.  小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解水生成氢气和氧气时,电能转化为化学能 | |
| B. | 煤燃烧时,化学能主要转化为热能 | |
| C. | 绿色植物进行光合作用时,太阳能转化为化学能 | |
| D. | 白炽灯工作时,化学能主要转化为光能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2和Cl2使品红溶液褪色的原理相同 | |
| B. | 浓硫酸分别使胆矾变白、蔗糖变黑时,浓硫酸表现的性质相同 | |
| C. | 浓硝酸和浓硫酸露置在空气中,浓度都降低的原因相同 | |
| D. | 浓硫酸与稀硫酸都能与金属锌反应放出气体,两个反应的氧化产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内压强不再发生变化 | |
| B. | v正(CO)=v正(H2O) | |
| C. | 生成n mol CO的同时,消耗n mol H2O | |
| D. | 1 mol H-H键断裂的同时,形成2 mol H-O键 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

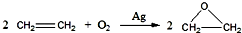
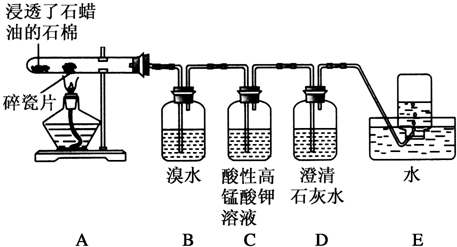
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
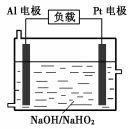 已知H2O2是一种弱酸,在强碱性溶液中主要以HO2-形式存在.目前研究比较热门的Al-H2O2燃料电池,其原理如图所示,电池总反应如下:
已知H2O2是一种弱酸,在强碱性溶液中主要以HO2-形式存在.目前研究比较热门的Al-H2O2燃料电池,其原理如图所示,电池总反应如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com