
| A、三者对应的氧化物均为酸性氧化物 |
| B、三者的单质直接与氧气反应都能生成两种以上氧化物 |
| C、同温度、同浓度的Na2CO3、NaNO3、Na2SO3溶液的pH:NaNO3<Na2SO3<Na2CO3 |
| D、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:

| A、t1℃时,物质的量浓度:甲=乙 |
| B、温度变化相同时,溶解度数值的变化量:甲>乙 |
| C、t2℃时,饱和溶液中溶质的质量分数:甲=乙 |
| D、相同质量的饱和溶液由t2℃降到t1℃时,析出的固体:甲<乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水能导电,所以氨气是电解质 |
| B、SO2的水溶液能导电,但是SO2是非电解质 |
| C、水溶液中NaHSO4=Na++HSO4- |
| D、FeCl3溶液为酸性,因为Fe3++3H2O=Fe(OH)3+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 甲组 | ①Al(OH)3 ②SiO2 ③FeCl3溶液 ④SO2 |
| 乙组 | a.NaOH溶液 b.浓HNO3 c.氨水 d.氯水 e.H2O2溶液 |
| A、① | B、② | C、③ | D、④ |
查看答案和解析>>
科目:高中化学 来源: 题型:

2- 7 |
2- 7 |
2- 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
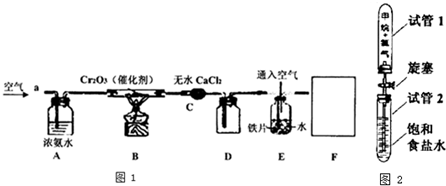
查看答案和解析>>
科目:高中化学 来源: 题型:
 氯化亚铜(Cu2Cl2)是一种重要的化工产品,常用作有机合成催化剂.已知:
氯化亚铜(Cu2Cl2)是一种重要的化工产品,常用作有机合成催化剂.已知:
查看答案和解析>>
科目:高中化学 来源: 题型:

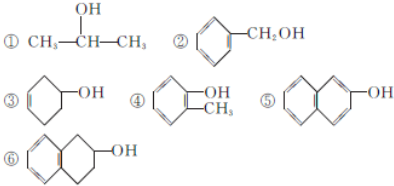
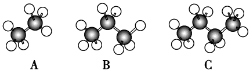
查看答案和解析>>
科目:高中化学 来源: 题型:
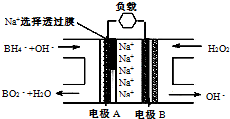 直接NaBH4/H2O2燃料电池(DBFC)的结构如右图,有关该电池的说法正确的是( )
直接NaBH4/H2O2燃料电池(DBFC)的结构如右图,有关该电池的说法正确的是( )| A、电极B材料中包含MnO2层,MnO2可起催化作用 |
| B、电池负极区的电极反应为:BH4-+8OH-+8e-=BO2-+6H2O |
| C、放电过程中,Na+ 从正极区向负极区迁移 |
| D、在电池反应中,每消耗1L 6 mol/LH2O2溶液,理论上流过电路中的电子为6NA个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com