
铝广泛应用于化学工业和日常生活中。工业上由铝土矿(Al2O3·3H2O的含量约为85%,其余主要为SiO2、Fe2O3等)冶炼金属铝的流程如下。
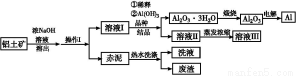
已知拜耳法生产Al2O3·3H2O的基本原理为:
Al2O3·3H2O+2NaOH(aq) 2NaAlO2(aq)+4H2O,[Al2O3·3H2O也可表示为2 Al(OH)3]
2NaAlO2(aq)+4H2O,[Al2O3·3H2O也可表示为2 Al(OH)3]
(1)操作Ⅰ的名称为 ,赤泥中除含有铝硅酸盐外,还含有的主要物质有 。
(2)为了提高铝土矿的溶出速率可采取的有效措施为 (任写三点)。
(3)用化学平衡理论解释稀释溶液Ⅰ有利于Al2O3·3H2O 结晶的原因 。
(4)为了析出Al2O3·3H2O,也可向溶液Ⅰ中通入过量CO2气体,写出生成Al2O3·3H2O的离子方程式: 。
(5)为了回收赤泥附着液带走的有用成分,工业上将用热水洗涤后的洗液用作溶液Ⅰ的稀释剂,请指出流程图中另一处类似的做法 。
(1)过滤 Fe2O3
(2)将铝土矿粉碎、加热、搅拌、增大NaOH的浓度(任答三点即可)
(3)稀释降低了NaOH的浓度,有利于NaAlO2的水解,使平衡向结晶方向移动(或向左移动)
(4)CO2(过量)+Al +2H2O
+2H2O Al(OH)3↓+HC
Al(OH)3↓+HC
或2CO2(过量)+2Al +4H2O
+4H2O Al2O3·3H2O↓+2HC
Al2O3·3H2O↓+2HC
【解析】流程原理分析如下:铝土矿(Al2O3、SiO2、Fe2O3)经NaOH溶液处理,Al2O3、SiO2转化为NaAlO2和铝硅酸盐,然后过滤,滤出Fe2O3和铝硅酸盐成为赤泥。对于NaAlO2溶液,用所给已知反应知经稀释,NaOH浓度降低,使NaAlO2的水解平衡向结晶方向移动(或向左移动),从而得到Al(OH)3(Al2O3·3H2O),然后煅烧去水得到Al2O3,电解熔融Al2O3得到金属Al。在促使Al(OH)3(Al2O3·3H2O)析出的过程中也可采取通入CO2气体的方法,通过反应CO2(过量)+Al +2H2O
+2H2O  Al(OH)3↓+HC
Al(OH)3↓+HC 得到Al(OH)3。溶液Ⅱ主要是析出Al(OH)3后,残留有NaAlO2的NaOH溶液,经蒸发浓缩可以继续溶解铝土矿。
得到Al(OH)3。溶液Ⅱ主要是析出Al(OH)3后,残留有NaAlO2的NaOH溶液,经蒸发浓缩可以继续溶解铝土矿。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源:2014高考化学名师选择题专练 实验基础练习卷(解析版) 题型:选择题
如图所示装置中,若关闭活塞,则品红溶液无变化,石蕊试液变红,澄清石灰水变浑浊。若打开活塞,则品红溶液褪色,石蕊试液变红,澄清石灰水变浑浊。据此判断该气体和广口瓶中盛放的物质分别是( )

A.CO2和浓H2SO4
B.SO2和NaHCO3溶液
C.Cl2和NaHCO3溶液
D.Cl2和饱和氯化钠溶液
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 元素周期表元素周期律练习卷(解析版) 题型:选择题
R、X、Y、M、Z五种短周期主族元素的原子半径依次减小,X、Y、Z的电子层数之和为5,X元素原子的最外层电子数是它的电子层数的2倍,Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,M是地壳中含量最多的元素,R与Z的最外层电子数相同。下列叙述正确的是( )
A.Z与M形成的化合物中不可能含有非极性键
B.对应氢化物的热稳定性:X>Y>M
C.单质的还原性:R>M>Y>X
D.X、Y、M、Z四种元素组成的离子化合物受热易分解
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 NA的应用练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.0.5 mol/L MgCl2溶液中Cl-的数目为NA
B.58 g乙烯和乙烷的混合气体中碳原子数目一定为4NA
C.常温常压下,22.4 L NO和N2的混合气体中分子数目大于NA
D.标准状况下,0.5 mol氦气含有的电子数为NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 物质结构与性质练习卷(解析版) 题型:填空题
已知:A、B、C、D、E、F是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2p轨道上只有两个电子,C元素的基态原子L层只有2对成对电子,D是元素周期表中电负性最大的元素,E2+的核外电子排布和Ar原子相同,F的核电荷数是D和E的核电荷数之和。
请回答下列问题:
(1)分子式为BC2的空间构型为 形;F2+的核外电子排布式为 。
(2)A分别与B、C形成的最简单化合物的稳定性B C(填“大于”或“小于”);A、C两元素可组成原子个数比为1∶1 的化合物,C元素的杂化类型为 。
(3)A2C所形成的晶体类型为 ;F单质形成的晶体类型为 。
(4)F元素氧化物的熔点比其硫化物的 (填“高”或“低”),请解释其原因
。
(5)E元素与C元素形成的化合物是 化合物,其晶体熔化时破坏的作用力是 ,晶体EC的熔点比晶体BC2的熔点 (填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 有机合成与推断练习卷(解析版) 题型:填空题
兔耳草醛是食品与化妆品工业中的香料添加剂。工业上可通过有机化工原料A制得,其合成路线如下图所示:
A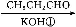 B
B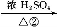 C
C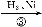 D
D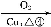
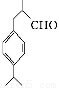 (兔耳草醛)
(兔耳草醛)
已知:①CH3CHO+CH3CHO CH3CH(OH)CH2CHO
CH3CH(OH)CH2CHO
②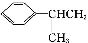 可写成
可写成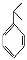
(1)B中含氧官能团的名称是 。
(2)上述合成路线中反应①属于 ,反应②属于 (填写反应类型)。
(3)写出由D获得兔耳草醛的化学反应方程式: 。
(4)A的同分异构体中符合以下条件的有 种。
a.能使FeCl3溶液显紫色
b.能发生加聚反应
c.苯环上只有两个互为对位的取代基
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 化学实验练习卷(解析版) 题型:实验题
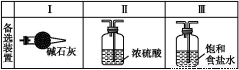
某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
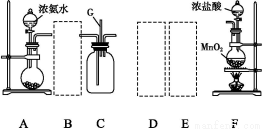
(1)装置F中发生反应的离子方程式为 。
(2)装置A中的烧瓶内固体可选用 (填以下选项的代号)。
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择,并将编号填入下列空格:B ,D ,E (均填编号)。
(4)氯气和氨气在常温下相混就会反应生成氯化铵和氮气,装置C内出现浓厚的白烟并在容器内壁凝结,请设计实验方案鉴定该固体就是氯化铵: 。
(5)从装置C的出气管口处逸出的尾气可能含有污染环境的气体,如何处理?
。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 选修3物质结构与性质练习卷(解析版) 题型:选择题
PH3是一种无色剧毒气体,其分子结构和NH3相似,但P-H键键能比N-H键键能低。下列判断中错误的是( )
A.PH3分子呈三角锥形
B.PH3分子是极性分子
C.PH3沸点低于NH3沸点,因为P—H键键能低
D.PH3分子稳定性低于NH3分子,因为N—H键键能高
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题8化学反应速率与化学平衡练习卷(解析版) 题型:选择题
可逆反应:A+3B 2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是( )
2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是( )
A.vD=0.4 mol/(L·s)B.vC=0.5 mol/(L·s)
C.vB=0.6 mol/(L·s)D.vA=0.15 mol/(L·s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com