
【题目】在密闭容器中,反应2X(g)+Y2(g)2XY(g);△H<0,达到甲平衡.在仅改变某一条件后,达到乙平衡,下列分析正确的是( )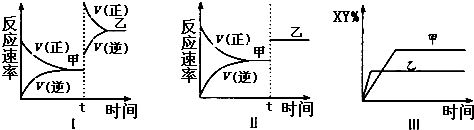
A.图I中,甲、乙的平衡常数分别为K1、K2 , 则K1<K2
B.图Ⅱ中,平衡状态甲与乙相比,平衡状态甲的反应物转化率低
C.图Ⅱ中,t时间是增大了压强
D.图Ⅲ是反应分别在甲、乙条件下达到平衡,说明乙温度高于甲
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子中的离子,能在溶液中大量共存的是( )
A.Na+、Mg2+、Cl-、OH-B.H+、Ca2+、CO32-、NO3-
C.Cu2+、K+、SO42-、NO3-D.Na+、H+、OH-、Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列实验事实:
①![]() 固体既能溶于
固体既能溶于![]() 溶液得到
溶液得到![]() 溶液,又能溶于硫酸得到
溶液,又能溶于硫酸得到![]() 溶液;
溶液;
②向![]() 溶液中滴加
溶液中滴加![]() 溶液,再酸化,可得
溶液,再酸化,可得![]() 溶液;
溶液;
③将![]() 溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是
A. 化合物![]() 中
中![]() 元素为+3价
元素为+3价
B. 实验①证明![]() 是两性氧化物
是两性氧化物
C. 实验②证明![]() 既有氧化性又有还原性
既有氧化性又有还原性
D. 实验③证明氧化性: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在水溶液中发生如下反应:①16H++10C-+2XO![]() ===2X2++5C2+8H2O;②2A2++B2===2A3++2B-;③2B-+C2===B2+2C-。下列说法错误的是( )
===2X2++5C2+8H2O;②2A2++B2===2A3++2B-;③2B-+C2===B2+2C-。下列说法错误的是( )
A. 反应C2+2A2+===2A3++2C-可以进行
B. 反应③是置换反应
C. 氧化性由强到弱的顺序是XO![]() >C2>B2>A3+
>C2>B2>A3+
D. 还原性由强到弱的顺序是C->A2+>B->X2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是最重要的氮肥,是产量最大的化工产品之一.德国人哈伯在1905年发明了合成氨的方法,其合成原理为:N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJmol﹣1 , 他因此获得了1918年诺贝尔化学奖. 在密闭容器中,使2mol N2和6mol H2混合发生下列反应:N2(g)+3H2(g)2NH3(g)(正反应为放热反应)
(1)当反应达到平衡时,N2和H2的转化率比是 .
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量 ,
密度 . (填“变大”“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将(填“正向”“逆向”或“不”)移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有①![]() 、
、![]() 、
、![]() ②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
②H2、D2、T2 ③石墨、金刚石④科学家们发现氢元素有三种同位素原子四组微粒或物质,回答下列问题:
(1)分别写出氢元素三种同位素的名称:______、_______、______。写出用做制造氢弹原料的同位素原子:______(填原子符号)。
(2)互为同位素的是________(填编号,下同)。
(3)互为同素异形体的是_______。
(4)由①和④中微粒能结合成三原子化合物,写出这些化合物的相对分子质量的最大值和最小值是_____________。
(5)质量相同的H216O 和D216O 所含质子数之比为_______,中子数之比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(![]() )是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产
)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产![]() 的主要流程如下:
的主要流程如下:
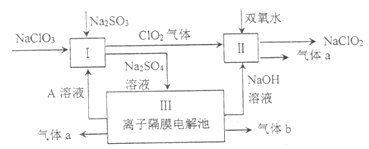
(1)I中发生反应的还原剂是________(填化学式)。
(2)II中反应的离子方程式是_________。
(3)III中离子隔膜电解池的装置如下:
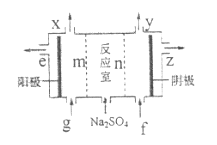
①A的化学式是_________,A在_________口产生。
②m为_______(填“阴”、“阳”)离子交换膜。
③结合化学用语和文字说明解释![]() 产生的原因:_________。
产生的原因:_________。
(4)![]() 是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:
是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备: ![]()
①该反应中氧化剂和还原剂的物质的量之比是_________。
②研究表明:若反应开始时盐酸浓度越大,则气体产物中![]() 的含量越大,运用氧化还原反应规律分析其原因是___________。
的含量越大,运用氧化还原反应规律分析其原因是___________。
(5)![]() 变质可分解为
变质可分解为![]() 和
和![]() 。取等质量变质前后的
。取等质量变质前后的![]() 试样均配成溶液,分别与足量
试样均配成溶液,分别与足量![]() 溶液反应时,消耗
溶液反应时,消耗![]() 的物质的量前者_______(填>、<、=)后者。
的物质的量前者_______(填>、<、=)后者。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com