
| A、所用NaOH已经潮解 |
| B、向容量瓶中加水未到刻度线 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、定容时仰视刻度线 |
| n |
| V |


科目:高中化学 来源: 题型:
| A、混合气体的压强 |
| B、混合气体的密度 |
| C、混合气体的相对分子质量 |
| D、C的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使用滤纸称量氢氧化钠固体 |
| B、溶解后未冷却直接定容 |
| C、容量瓶不干燥,存有少量蒸馏水 |
| D、胶头滴管加水定容时仰视刻度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、定容时俯视刻度线 |
| B、没有洗涤烧杯和玻璃棒 |
| C、用托盘天平称量0.6gNaCl固体 |
| D、配制前容量瓶中残留少量的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、卤化氢分子中,卤素的非金属性越强,共价键的极性也越大,稳定性也越强 |
| B、H2O中O-H键之间的键角大于H2S中S-H键之间的键角 |
| C、具有极性键且空间构型不对称的A2B或AB2型分子为极性分子 |
| D、非极性分子中只存在非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
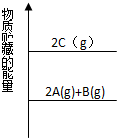
| A、C(g)=A(g)+1/2B(g)△H<0 |
| B、2C=2A+B△H>0 |
| C、2A+B=2C△H>O |
| D、A(g)+1/2B(g)=C(g)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
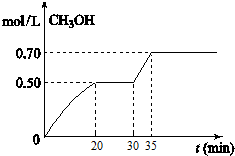
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:A<B<C |
| B、三种元素的最高价氧化物对应水化物均可由化合反应得到 |
| C、A的氢化物稳定性大于C的氢化物稳定性 |
| D、单质B与A的最高价氧化物不能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
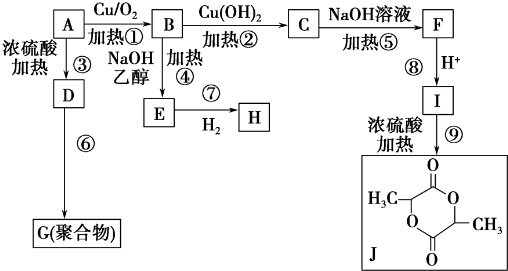
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com