
【题目】矿泉水瓶上的部分说明文字,列出了饮用天然水理化指标,这里的钙、钾、钠是指( )
A.原子
B.分子
C.单质
D.元素
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】可逆反应2SO2(g)+O2(g)![]() 2SO3(g)△H<0,在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间的关系如图所示.下列说法正确的是( )
2SO3(g)△H<0,在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间的关系如图所示.下列说法正确的是( )

A. 维持温度、容积不变,t1时充入SO3(g)
B. 维持压强不变,t1时升高反应体系温度
C. 维持温度、容积不变,t1时充入一定量Ar
D. 维持温度、压强不变,t1时充入SO3(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =__________________。
(2)该反应为__________反应(“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_______________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.如图所示为常见玻璃仪器的部分结构:
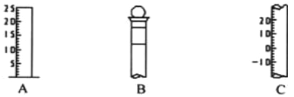
(1)请写出所列仪器的名称: A______,B_______,C_______;
(2)仪器 B 使用前必须__________________。
(3)仪器 B 上标记有______(填序号);①质量 ②温度 ③刻度线 ④浓度 ⑤容积
II.已知某“84 消毒液”瓶体部分标签如图所示,该“84 消毒液”通常稀释 100 倍(体积之比)后使用。请回答下列问题:
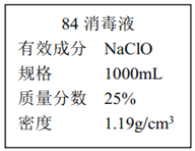
(1)该“84 消毒液”的物质的量浓度约为_______mol·L-1。(保留两位有效数字)
(2)某同学取100 mL该“84 消毒液”,稀释后用于消毒,稀释后的溶液中 c (Na+)=_____。
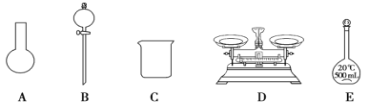
(3)该同学参阅该“84 消毒液”的配方,欲用 NaClO 固体配制 250 mL含 NaClO 质量分数为 25%的消毒液。下列说法不正确的是________(填序号)。
a.如图所示的仪器中,有三种是不需要的,还需要其它玻璃仪器
b.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
c.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
(4) “84 消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用 98%(密度为1.84g·cm-3)的浓硫酸配制2 L 2.3 mol·L-1 的稀硫酸用于增强“84 消毒液”的消毒能力。需用浓硫酸的体积为______ mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在空气中,有下列反应发生: ①N2 + O2 = 2NO;②2NO+O2=2NO2;③3NO2 + H2O = 2HNO3 + NO;④ 2SO2+O2 = 2SO3;⑤ SO3 + H2O = H2SO4; ⑥SO2+H2O![]() H2SO3; ⑦3O2 = 2O3,其中属于氧化还原反应的是( )
H2SO3; ⑦3O2 = 2O3,其中属于氧化还原反应的是( )
A. ①②③④ B. ①②③④⑦ C. ①②④⑦ D. ①②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的三种酸HX、HY、HZ的溶液,其pH依次为4、5、6,则KX、KY、KZ的碱性由强到弱的顺序是( )
A. KX、KZ、KY B. KX、 KY、KZ
C. KZ、KY 、KX D. KY、KZ、KX
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果汁中含有Fe2+ , 现榨的苹果汁在空气中会由浅绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有( )
A.氧化性
B.还原性
C.碱性
D.酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:4NH3(g)+6NO(g)=5N2(g)+6H2O(l) ΔH1 4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH2
则 NH3(g)的标准燃烧热Δ H=__________________。
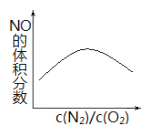
(2)高温下,N2(g)+O2(g)![]() 2NO(g), ΔH<0,反应达到平衡时混合气体中NO的体积分数与反应物中 c(N2)/c(O2)的比值的关系如图,请在右图上画出适当降温后,反应达到平衡时混合气体中 NO 的体积分数与反应物中 c(N2)/c(O2)的比值的关系图。_______
2NO(g), ΔH<0,反应达到平衡时混合气体中NO的体积分数与反应物中 c(N2)/c(O2)的比值的关系如图,请在右图上画出适当降温后,反应达到平衡时混合气体中 NO 的体积分数与反应物中 c(N2)/c(O2)的比值的关系图。_______
(3)工业上电解Na2CO3溶液可以生成NaHCO3和NaOH两种工业重要原料,装置如图所示。
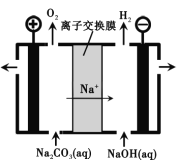
①电解的总反应式___________________________。
②已知H2CO3的Ka1=4.30×10-7, Ka2=5.60×10-11, 当同浓度的稀NaHCO3和稀Na2CO3溶液以2∶1体积比混合后,混合液的c(H+)约为____________ mol·L-1。
(4)为测定某NaNO2 溶液的物质的量浓度, 准确量取10.00mLNaNO2 溶液样品与24.00mL 0.05000mol·L-1 过量的酸性KMnO4 溶液充分反应,反应后所得溶液用0.1000mol/L(NH4)2Fe(SO4)2 标准溶液滴定至终点,消耗(NH4)2Fe(SO4)2 溶液 10.00mL。 终点的现象_____________________,通过计算确定NaNO2 溶液的物质的量浓度___________ mol·L-1。
有关反应式:5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O; 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com