
| A.在无色透明溶液中:Al3+、Na+、HCO3-、Cl- |
| B.在能使甲基橙呈红色的溶液中:Mg2+、NH4+、Fe2+、I- |
| C.加入铝粉放出氢气的溶液: K+、Ca2+、NO3-、SO42- |
| D.在水电离产生的H+的浓度为1×10-13mol?L-1的溶液:Cu2+、Na+、NO2-、SO42- |
科目:高中化学 来源:不详 题型:填空题
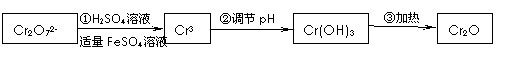
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.0.1mol/LNaHCO3溶液中,c(OH-)-C(H+)=c(H2CO3)-c(CO32-) | B.A+和B-的电子层结构相同,则A原子的核电荷数比B原子的小 | C.A盐的溶解度在同温下比B盐的大,则A盐溶液的物质的量浓度比B盐溶液的大 | D.A原子失去的电子比B原子的多,则A单质的还原性比B单质的强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
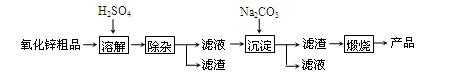
| 沉淀物 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Fe(OH)2 |
| pH | 3.2 | 6.7 | 8.0 | 9.7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g) + H2(g) △H=_____________。
CO2(g) + H2(g) △H=_____________。 CO2(g)+H2(g) K=1.0。则平衡后CO的转化率为_______,平衡混合物中H2的体积分数为_______。
CO2(g)+H2(g) K=1.0。则平衡后CO的转化率为_______,平衡混合物中H2的体积分数为_______。 _____________。
_____________。 (g) = CH3OH (g),在一定条件下,该反应在一个密闭容器中达到平衡,若维持c(H2)和容器的温度不变,
(g) = CH3OH (g),在一定条件下,该反应在一个密闭容器中达到平衡,若维持c(H2)和容器的温度不变, 增大容器的体积,则平衡_________(填字母)
增大容器的体积,则平衡_________(填字母)| A.不移动 | B.向正反应方向移动 |
| C.向逆反应方向移动 | D.无法判断移动的方向 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 检验,得PH="1" 可知该溶液有强酸性
检验,得PH="1" 可知该溶液有强酸性查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,均为强电解质,它们的阳离子有Al3+、NH+4、Na+、Ag+、H+五种,阴离子有Cl-、HCO-3、OH-、NO-3、SO2-4五种,现将它们分别配成0.lmol/L。的溶液,进行如下实验:
,均为强电解质,它们的阳离子有Al3+、NH+4、Na+、Ag+、H+五种,阴离子有Cl-、HCO-3、OH-、NO-3、SO2-4五种,现将它们分别配成0.lmol/L。的溶液,进行如下实验:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在含等物质的量的HCO3?、OH?、CO32?的溶液中,逐滴加入盐酸:OH?、HCO3?、CO32? |
| B.在含等物质的量的Al3+、H+、NH4+的溶液中,逐滴加入NaOH溶液:NH4+H+、Al3+、Al(OH)3 |
| C.在含等物质的量的I?、Br? 、SO32?的溶液中,缓慢通入Cl2: Br? 、I?、SO32? |
| D.在含等物质的量的Fe3+、Cu2+、H+的溶液中,加入Zn:Fe3+、Cu2+、H+、Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com