
炼铁的还原剂CO是由焦炭和CO2反应而得。现将焦
炭和CO2放入体积为2 L的密闭容器中,高温下进行
 下列反应:C(s)+CO2(g)
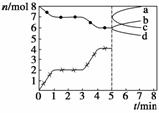
下列反应:C(s)+CO2(g)  2CO(g) ΔH=Q kJ·mol-1。右图为CO2、CO的物质的量n随时间t的变化关系图:
2CO(g) ΔH=Q kJ·mol-1。右图为CO2、CO的物质的量n随时间t的变化关系图:
下列说法正确的是( )
A.0~1 min,v(CO)=1 mol·L-1·min-1;1~3 min时,v(CO)=v(CO2)
B.当容器内的压强不变时,反应一定达到平衡状态,且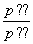 <1
<1
C.3 min时温度由T1升高到T2,则Q>0,再达平衡时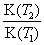 =4.7
=4.7
D.5 min时再充入一定量的CO,a、b曲线分别表示n(CO)、n(CO2)的变化
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
对下面符号或示意图的理解,正确的是( )
A.Fe2+、Fe3+都属于铁元素,是同一种离子
B.NO2、N2O4中氮元素的化合价都是+4价,是同一化合物
C.NH4NO3中氮元素有两种不同的化合价,分别是-3、+5
D.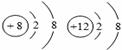 两种粒子的电子排布情况相同,属于同一元素
两种粒子的电子排布情况相同,属于同一元素
查看答案和解析>>
科目:高中化学 来源: 题型:
研究化肥的合成、废水的处理等有现实的重要意义。
Ⅰ.尿素是一种非常重要的高氮化肥,工业上合成尿素的反应如下:
2NH3(l)+CO2(g) H2O(l)+H2NCONH2 (l) △H=-103.7 kJ·mol-1
H2O(l)+H2NCONH2 (l) △H=-103.7 kJ·mol-1
试回答下列问题:
(1)下列措施中有利于提高尿素的产率的是___________。
A.采用高温 B.采用高压 C.寻找更高效的催化剂
(2)合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g) H2NCOONH4(氨基甲酸铵) (l) △H1
H2NCOONH4(氨基甲酸铵) (l) △H1
第二步:H2NCOONH4(l) H2O(l)+H2NCONH2(l) △H2
H2O(l)+H2NCONH2(l) △H2
某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:
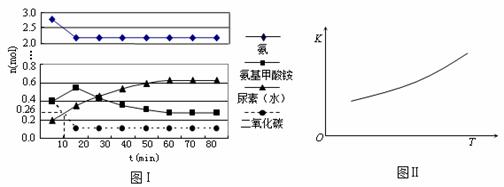
① 已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_____步反应决定。
② 反应进行到10 min时测得CO2的物质的量如图Ⅰ所示,则用CO2表示的第一步反应的速率v(CO2)=____________________
③ 第二步反应的平衡常数K随温度的变化如上右图Ⅱ所示,则△H2 0
(填“>”“<”或“=”)
Ⅱ.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表。
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As |
| 浓度 | 28.42 g/L | 1.6 g·L-1 |
| 排放标准 | pH 6~9 | 0.5 mg·L-1 |
表1.几种砷酸盐的Ksp 表2.工厂污染物排放浓度及允许排放标准
回答以下问题:
(3)若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol·L-1,
c(AsO43-)最大是 mol·L-1。
(4)工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式 。
(5)在处理含砷废水时采用分段式,先向废水中投入适量生石灰调节pH到2,再投入适量生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
① 将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为 ;
②在pH调节到8左右才开始出现大量Ca3(AsO4)2沉淀的原因为
查看答案和解析>>
科目:高中化学 来源: 题型:
在0.lmol/L的HA溶液中存在如下电离平衡: HA A-+H+,对于该溶液,下列叙述正确的是
A-+H+,对于该溶液,下列叙述正确的是
A.滴加少量0.lmol/L HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减少
B.加水,溶液中所有离子浓度均减小
C.加入少量NaA固体,平衡向逆反应方向移动,溶液中c(OH-)增大
D.加入少量NaOH固体,平衡向正反应方向移动, 溶液中c(H+)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是
A. 2NO2  N2O4 (正反应为放热反应)
N2O4 (正反应为放热反应)
B. C(s)+ CO2  2CO (正反应为吸热反应)
2CO (正反应为吸热反应)
C. N2 + 3H2  2NH3 (正反应为放热反应)
2NH3 (正反应为放热反应)
D. H2S  H2 + S(s)(正反应为吸热反应)
H2 + S(s)(正反应为吸热反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,0.1 mol/L某一元酸(HA)溶液中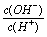 =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
A.溶液中水电离出的c(H+)=10-10 mol/L
B.溶液中c(H+)+c(A-)=0.1 mol/L
C.溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大
D.与0.05mol/L NaOH溶液等体积混合后所得溶液中离子浓度大小关系为
c(A-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
①正常雨水的PH为7.0,酸雨的PH小于7.0。
②严格执行机动车尾气排放标准有利于防止大气污染
③使用二氧化硫和某些含硫化合物进行增白的食品会对人体健康产生损害
④使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害
⑤食品厂产生的含丰富氮、磷营养素的废水可长期排向水库养鱼
A、①②③ B、①④⑤ C、②③④ D、③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若A、B相连,A为负极;C、D相连,D上有气泡逸出;A、C相连A极减轻;B、D相连,B为正极。则四种金属的活泼性顺序由大到小排列为( )
A. A>C>D>B B. A>C>B>D C. B>D>C>A D. A>B>C>D
查看答案和解析>>
科目:高中化学 来源: 题型:
用50 mL 0.55 mol/L盐酸与50 mL 0.50 mol/L NaOH溶液进行中和热测定的实验,测量结果偏高的原因可能是( )
A.实验装置保温、隔热效果差
B.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
C.量取NaOH溶液的体积时仰视读数
D.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com