
| A. | Mg2+、H+、Zn2+、SO42- | B. | Na+、Ba2+、OH-、SO42- | ||
| C. | MnO4-、K+、H+、SO42- | D. | K+、NO3-、OH-、Na+ |
分析 无色溶液可排除Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,与NH4HCO3作用能产生气体,溶液可能呈酸性或碱性,
A.四种离子之间不反应,都是无色离子,且都不与氢离子反应;
B.钡离子与硫酸根离子反应生成硫酸钡沉淀;
C.高锰酸根离子为有色离子;
D.四种离子之间不反应,都是无色离子,且都不与氢氧根离子反应.
解答 解:溶液无色可排除Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,与NH4HCO3作用能产生气体,溶液可能呈酸性或碱性,溶液中存在大量的氢氧根离子和氢离子,
A.Mg2+、H+、Zn2+、SO42-之间不发生反应,都不与H+反应,在酸性溶液中能够大量共存,故A正确;
B.Ba2+、SO42-之间反应生成难溶物硫酸钡,在溶液中不能大量共存,故B错误;
C.MnO4-为有色离子,不满足溶液无色的条件,故C错误;
D.K+、NO3-、OH-、Na+之间不反应,都是无色离子,都不与氢氧根离子反应,在碱性溶液中能够大量共存,故D正确;
故选AD.
点评 本题考查离子共存的判断,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;是“可能”共存,还是“一定”共存等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
 我国首创的海洋电池以铝板、铂网为电极,以海水作为电解质溶液,电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列有关该电池说法正确的是( )
我国首创的海洋电池以铝板、铂网为电极,以海水作为电解质溶液,电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列有关该电池说法正确的是( )| A. | 该电池工作时将电能转化为化学能 | |
| B. | 通常一段时间后该电池只需更换铝板就可继续使用 | |
| C. | 负极反应式是:O2+2H2O+4e-=4OH- | |
| D. | 铝片发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
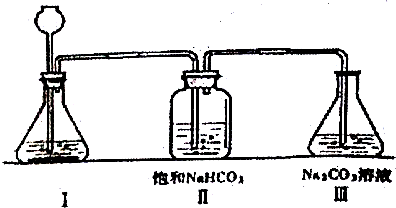
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4 原子半径最大的是① | |
| B. | 具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4第一电离能最大的是④ | |
| C. | ①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数增大而递增的是④ | |
| D. | 某元素气态基态原子的逐级电离能(kJ•mol-1)分别为738、1 451、7 733、10 540、13 630、17 995、21 703,当它与氯气反应时可能生成的阳离子是X3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com