
对于锌-铜-稀硫酸组成的原电池装置中,当导线中有1mol电子通过时,理论上的两极变化是: ①锌片溶解了32.5g;②锌片增重了32.5g; ③铜片上析出1gH2;④铜片上析出1mol H2;
A. ①和③ B.①和④ C.②和③ D.②和④
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
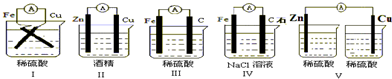
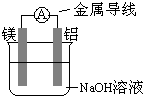
查看答案和解析>>
科目:高中化学 来源: 题型:
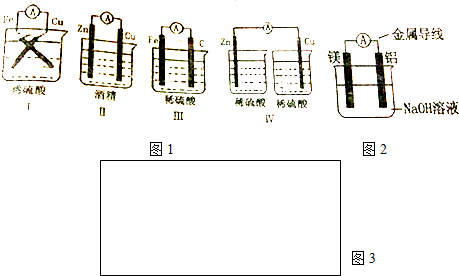
查看答案和解析>>
科目:高中化学 来源:2013届江西省高一下学期第一次月考化学试卷 题型:选择题
对于锌-铜-稀硫酸组成的原电池装置中,当导线中有1mol电子通过时,理论上的两极变化是
①锌片溶解了32.5g ②锌片增重32.5g ③铜片上析出lg H2 ④铜片上析出1mol H2
A.①和③ B.①和④ C.②和③ D.②和④
查看答案和解析>>
科目:高中化学 来源:2013届江西省高一下学期期中考试化学试卷 题型:选择题
对于锌-铜-稀硫酸组成的原电池装置中,当导线中有1mol电子通过时,理论上的两极变化是: ①锌片溶解了32.5g; ②锌片增重了32.5g; ③铜片上析出1gH2;④铜片上析出1mol H2;
A. ①和③ B.①和④ C.②和③ D.②和④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com