
学生甲和学生乙完成了下列实验,其中实验现象完全相同的是( )
学生甲 学生乙
A 向碳酸氢钠溶液中逐渐加入盐酸 向盐酸中逐滴加入碳酸氢钠溶液
B 向氯化亚铁溶液中滴加KSCN溶液,再通入氯气 向氯化亚铁溶液中通入氯气,再滴加KSCN溶液
C 向三氯化铝溶液中滴加氢氧化钠溶液 向氢氧化钠溶液中滴加入三氯化铝溶液
D 向BaCl2溶液中通入二氧化硫 向BaCl2溶液中通入SO3
A. A B. B C. C D. D
考点: 化学实验方案的评价;二氧化硫的化学性质;钠的重要化合物;镁、铝的重要化合物;铁的氧化物和氢氧化物.
专题: 实验评价题;元素及其化合物.
分析: A.碳酸氢钠和盐酸反应生成二氧化碳气体;
B.氯化亚铁可被氯气氧化,但氯化亚铁与KSCN不发生反应;
C.向三氯化铝溶液中滴加氢氧化钠溶液,先生成沉淀,氢氧化钠过量时沉淀溶解,但向氢氧化钠溶液中滴加入三氯化铝溶液,先没有沉淀生成;
D.氯化钡和二氧化硫不反应.
解答: 解:A.均发生碳酸氢根离子与氢离子的反应,均观察到气泡生成,故A正确;
B.向FeCl2溶液中滴加KSCN溶液,再通入Cl2先不变色后变红,向FeCl2溶液中通入Cl2,再滴加KSCN溶液变红色,现象不同,故B错误;
C.向三氯化铝溶液中滴加氢氧化钠溶液先生成沉淀后沉淀消失,而向氢氧化钠溶液中滴加入三氯化铝溶液,开始没有沉淀后生成沉淀,现象不同,故C错误;
D.向BaCl2溶液中通入SO2不反应,向BaCl2溶液中通入SO3反应生成硫酸钡沉淀,现象不同,故D错误.
故选A.
点评: 本题考查化学实验方案的评价,侧重物质性质的考查,明确物质之间的反应为解答本题的关键,注意反应与现象的关系,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
25℃时,水的电离达到平衡:H2O⇌H++OH﹣△H>0,下列叙述正确的是( )
|
| A. | 向水中加入氨水,平衡逆向移动,c(OH﹣)降低 |
|
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
|
| C. | 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
|
| D. | 将水加热,KW增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
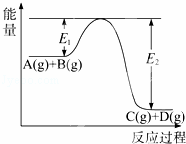
反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
(1)该反应是 反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率 (填“增大”“减小”“不变”),原因是 ;
(3)反应体系中加入催化剂对反应热是否有影响? ,原因是 ;
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 ,E2 (填“增大”“减小、”“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W、Q、R均为前四周期元素,且原子序数依次增大.其相关信息如下表所示:
X的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同
Y元素的族序数是周期序数的三倍
Z元素的电负性在所有元素中最大
W原子的第一至第六电离能分别为:I1=578KJ•mol﹣1,I2=1817KJ•mol﹣1,I3=2745KJ•mol﹣1,I4=11575KJ•mol﹣1,I5=14830KJ•mol﹣1,I6=18376KJ•mol﹣1
Q为前四周期中电负性最小的元素
R原子最高能层上只有1个单电子,其余各能层均已充满电子.
请回答:
(1)R在周期表中位于 区,写出R基态原子的价电子排布式 .
(2)X与Y形成的二元化合物中属于非极性分子的 (用化学式表示).
(3)写出Z元素的单质与水反应的方式 ,此反应中氧化剂与氧化产物物质的量之比为 .
(4)X的氯化物的熔点比Q的氯化物的熔点 (“高”或“低”),理由是 .
(5)光谱证实单质W与强碱性溶液反应有[W(OH)4]﹣生成,则中[W(OH)4]﹣﹣存在 (填选项字母)
a.极性共价键 b.非极性共价键 c.配位键 d.σ键 e.π键
(6)金刚砂(SiC)的结构与金刚石(4个碳原子在立方体体内,其余碳原子分别位于面心和顶角)相似,硬度与金刚石相当,则金刚砂的晶胞中含有 个硅原子, 个碳原子,其中硅原子的杂化方式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
将足量的CO2通入下列各溶液中,所含离子还能大量共存的是( )
A. K+、SiO32﹣、Cl﹣、NO3﹣ B. H+、NH4+、Al3+、SO42﹣
C. Na+、S2﹣、OH﹣、SO42﹣ D. Na+、CO32﹣、CH3COO﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子或分子组在溶液中能大量共存的是( )
A. K+ NO3﹣ I﹣ H2SO3
B. Na+ Fe3+ NO3﹣ SCN﹣
C. K+ AlO2﹣ CO32﹣ Al3+
D. NH4+ Mg2+ SO42﹣ CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
回答下列问题:
(1)氢氧化铝Al(OH)3是一种治疗胃酸(含盐酸)过多的药物,用化学方程式表示该反应的原理:
(2)炒菜时,经常加入少量的料酒(含乙醇)和醋(含乙酸),可使菜变得香醇可口,用化学方程式表示该反应的原理: .
(3)工业上在一定条件下电解熔融氯化钠制取金属钠,写出该反应的化学方程式:
(4)CH4与Cl2在光照条件下能生成CH3Cl,写出该反应的化学方程式:
(5)向硫酸亚铁溶液中滴入氢氧化钠溶液,生成的灰白色沉淀迅速变成灰绿色,最后变成红褐色,此过程中涉及的氧化还原反应的化学方程式为: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com