
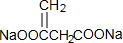 +NaCl+3H2O��
+NaCl+3H2O��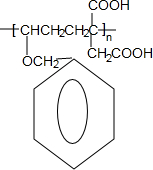 ��
�� ��
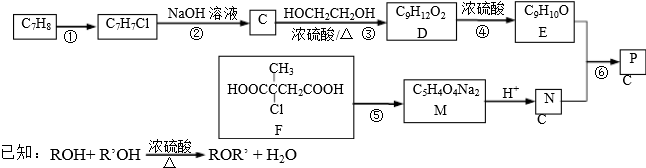
������ ��C7H8������Ӧ�����ɵ�C7H7Cl�ܹ���NaOH��Һ�з�Ӧ��֪��C7H8Ϊ�ױ����ױ��ڹ��������£����ϵ���ԭ�ӱ���ԭ��ȡ����C7H7ClΪ ��CΪ���״��������֪��Ӧ�ͷ�Ӧ������֪��DΪ
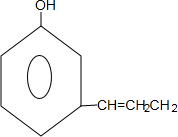
��CΪ���״��������֪��Ӧ�ͷ�Ӧ������֪��DΪ ��D��E����Ũ���������´�����ȥ��Ӧ����EΪ
��D��E����Ũ���������´�����ȥ��Ӧ����EΪ ����M�ķ���ʽ��֪��F��M��������ȥ��Ӧ���кͷ�Ӧ��MΪ
����M�ķ���ʽ��֪��F��M��������ȥ��Ӧ���кͷ�Ӧ��MΪ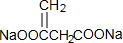 ��NΪ
��NΪ ��E��N�����Ӿ۷�Ӧ�õ��߾���P��PΪ
��E��N�����Ӿ۷�Ӧ�õ��߾���P��PΪ ���ݴ˷�����
���ݴ˷�����
��� �⣺��1����F�Ľṹ��ʽ��֪��F�к��еĹ��������Ȼ�����ԭ�ӣ���Ӧ�ٵķ�Ӧ����Ϊ���գ��ʴ�Ϊ���Ȼ�����ԭ�ӣ����գ�
��2��F��M��������ȥ��Ӧ���кͷ�Ӧ��MΪ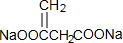 ����Ӧ�Ļ�ѧ����ʽΪ��HOOCCCl��CH3��CH2COOH+3NaOH$��_{��}^{�Ҵ�}$
����Ӧ�Ļ�ѧ����ʽΪ��HOOCCCl��CH3��CH2COOH+3NaOH$��_{��}^{�Ҵ�}$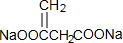 +NaCl+3H2O���ʴ�Ϊ��HOOCCCl��CH3��CH2COOH+3NaOH$��_{��}^{�Ҵ�}$
+NaCl+3H2O���ʴ�Ϊ��HOOCCCl��CH3��CH2COOH+3NaOH$��_{��}^{�Ҵ�}$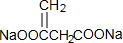 +NaCl+3H2O��
+NaCl+3H2O��
��3��EΪ ��NΪ
��NΪ ��E��N�����Ӿ۷�Ӧ�õ��߾���P��PΪ
��E��N�����Ӿ۷�Ӧ�õ��߾���P��PΪ ��
��
�ʴ�Ϊ�� ��
��
��4��EΪ ����ͬ���칹����Тٷ�����ֻ�б���һ����״�ṹ���ұ�����������ȡ��������1mol���л�������ˮ��Ӧʱ����4molBr2�����ʵĽṹ��ʽ������
����ͬ���칹����Тٷ�����ֻ�б���һ����״�ṹ���ұ�����������ȡ��������1mol���л�������ˮ��Ӧʱ����4molBr2�����ʵĽṹ��ʽ������ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��5���÷���ʽΪC5H8����Ϊ��Ҫԭ�ϣ��Ʊ�F�ĺϳ�·������ͼΪCH2=C��CH3��CH=CH2$\stackrel{��ˮ}{��}$CH2BrC��CH3��=CHCH2Br$��_{��}^{NaOH��Һ}$HOCH2C��CH3��=CHCH2OH$\stackrel{������}{��}$OHCC��CH3��=CHCHO$\stackrel{������}{��}$HOOCC��CH3��=CHCOOH$��_{����}^{HCl}$F��
�ʴ�Ϊ��CH2=C��CH3��CH=CH2$\stackrel{��ˮ}{��}$CH2BrC��CH3��=CHCH2Br$��_{��}^{NaOH��Һ}$HOCH2C��CH3��=CHCH2OH$\stackrel{������}{��}$OHCC��CH3��=CHCHO$\stackrel{������}{��}$HOOCC��CH3��=CHCOOH$��_{����}^{HCl}$F��
���� ���⿼�����л��ƶ���ϳɣ�ע������л���Ĺ����źͷ�Ӧ��������������Ĺؼ��Ǿ�F�Ľṹ��ʽ��D�ķ���ʽ�����жϣ���Ŀ�ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
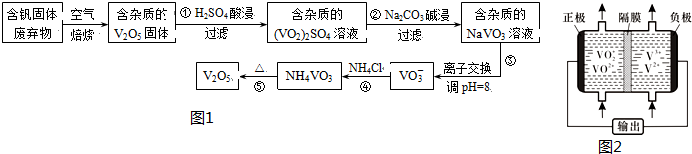
| ���� | V2O5 | NH4VO3 | VOSO4 | ��VO2��2SO4 |
| �ܽ��� | ���� | ���� | ���� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 10 | 20 | 30 | 40 | 50 | 70 |
| ��NH4��2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4•7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| Ħ���� | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
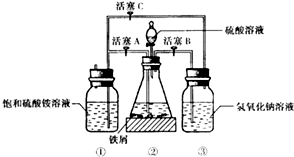
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
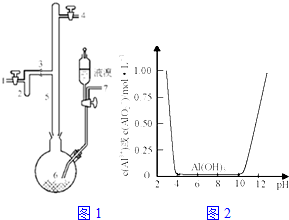 ���÷���������Ҫ�ɷ�ΪAl��������Fe��Si�ȣ��ȿ���ȡ�л��ϳɴ���AlBr3�ֿ���ȡ��ˮ�����������壮
���÷���������Ҫ�ɷ�ΪAl��������Fe��Si�ȣ��ȿ���ȡ�л��ϳɴ���AlBr3�ֿ���ȡ��ˮ�����������壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʱ��̫�� | B�� | ��Ӧ��ȴ���ٵ���AgNO3��Һ | ||
| C�� | ��AgNO3��Һǰδ��ϡHNO3�ữ | D�� | ��AgNO3��Һ��δ��ϡHNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
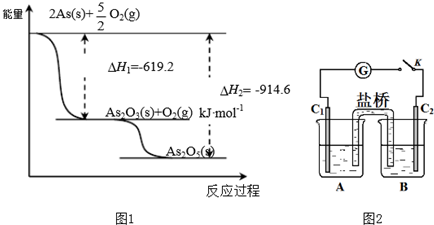
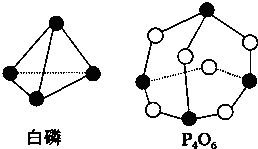 ��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJ/mol����P-P��198��P-O��360��O=O��498����ӦP4�����ף�+3O2�TP4O6�ķ�Ӧ�ȡ�HΪ��������
��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJ/mol����P-P��198��P-O��360��O=O��498����ӦP4�����ף�+3O2�TP4O6�ķ�Ӧ�ȡ�HΪ��������| A�� | -1 638 kJ/mol | B�� | +1 638 kJ/mol | C�� | -126 kJ/mol | D�� | +126 kJ/mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com