
【题目】已知下列各种元素中A,B两元素的原子序数,其中可形成AB2型离子化合物的是( )
①6和8 ②12和17 ③20和9 ④11和17.
A.①③
B.①②
C.②③
D.③④
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3 . Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用该原理处理污水,设计装置如图所示.下列说法正确的是( )

A. 为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环的物质A为CO2
B. 甲装置中阴极的反应为Fe﹣2e﹣═Fe2+
C. 为了增加污水的导电能力,应向污水中如入适量的NaOH溶液
D. 当乙装置中有1.6 g CH4参加反应,则C电极理论上生成气体在标准状况下为4.48 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物在生产、生活中有着重要的应用价值。请按要求回答下列问题。
(1)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理.

通过计算,可知系统(Ⅰ)和系统(Ⅱ) 制氢的热化学方程式分别为_________;_________;制得等量H2所需能量较少的是系統_________。
(2)H2S 与CO2在高温下发生反应: H2S(g)+CO2(g) ![]() COS(g)+H2O(g)。在340℃时,将0.10molCO2与0.10molH2S充入2.5 L的空钢瓶中。
COS(g)+H2O(g)。在340℃时,将0.10molCO2与0.10molH2S充入2.5 L的空钢瓶中。
①该反应平衡后H2O(g)的物质的量分数为0.3,H2S的平衡转化率α1=____,反应平衡常数K=____。
②在350℃重复试验,平衡后H2O(g)的物质的量分数为0.4,H2S的转化率α2_____α1,(填“>”“<”或“=”)该反应的△H____0。
③测定钢铁中硫含量: 将钢铁中的硫转化为H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为____,滴定反应的离子方程式为__________。
已知25 ℃时,H2SO3的电离常数K.a1=1×10-2,Ka2=5×10-8,则该温度下NaHSO3的水解平衡常数Kb=_____。若向NaHSO3溶液中加入少量的I2,则溶液中c(H2SO3)/c(HSO3-)将_______(填“增大”、“减小”或“不变" ).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为: ![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.苹果酸能被氧化成三元羧酸
B.1 mol苹果酸可与3 mol NaOH发生中和反应
C.含1 mol苹果酸的稀溶液与足量金属Na反应生成1.5molH2
D.2分子苹果酸相互反应,可形成结构为六元环、七元环或八元环的酯类物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象与结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | 向FeCl3和KSCN混合溶液中,加入少量KCl的固体 | 溶液颜色变浅 | FeCl3+3KSCN |
B | 用乙醇与浓硫酸反应制乙烯,将产生的气体直接通入酸性高锰酸钾溶液中 | 高锰酸钾溶液的紫红色褪去 | 乙烯能被酸性高锰酸钾氧化 |
C | 向装有X溶液的试管中滴入浓NaOH溶液,将干燥的红色石蕊试纸置于试管口 | 无明显现象 | X溶液中无NH4+ |
D | 常温下,向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞 | 变红,前者 红色更深 | 结合质子的能力:CO32- > HCO3- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氢有(1H,2H,3H)三种同位素,氯有(35Cl,37Cl)两种同位素.用“精确的天平”分别称量1000个HCl分子,所得数据可能有( )
A.1种
B.5种
C.6种
D.1000种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知金属钠与两种卤族元素形成的化合物Q、P,它们的晶格能分别为923 kJ·mol-1、786 kJ·mol-1,下列有关说法中不正确的是( )
A. Q的熔点比P的高 B. 若P是NaCl,则Q一定是NaF
C. Q中成键离子核间距较小 D. 若P是NaCl,则Q可能是NaBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知分解反应2N2O5(g)![]() 4NO2(g) + O2(g)的速率方程式v = k·cm(N2O5),k是与温度有关的常数,实验测定340K时的有关数据及根据相关数据做出的图像如下:
4NO2(g) + O2(g)的速率方程式v = k·cm(N2O5),k是与温度有关的常数,实验测定340K时的有关数据及根据相关数据做出的图像如下:
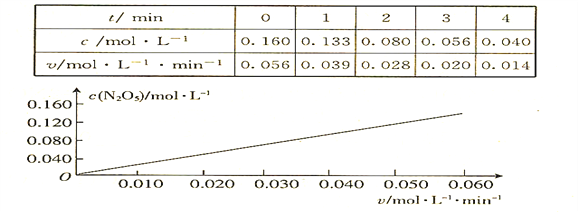
依据图表中的有关信息,判断下列有关叙述中不正确的是
A. 340K时,速率方程式中的m = 1
B. 340K时,速率方程式中的k = 0.350 min-1
C. 340K时,c(N2O5)= 0.100 mol·l-1时,v = 0.035 mol·l-1 ·min-1
D. 340K时,压强增大一倍,逆反应速率不变,正反应速率是原来的2倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com