
����Ŀ��������(AlN)��һ�����ͷǽ������ϣ��������ܻ���ˮ�⡣���������ڵ�����Χ��1700��ϳɣ�����Ϊ��ɫ������ɫ��ĩ��ijС��̽����ʵ�����Ʊ�AlN���ⶨ��Ʒ���ȣ����ʵ�����¡���ش�
(һ)�Ʊ�AlN

(1)�������������ҵķ�������װ�õ���ȷ����˳��Ϊj��__________________��i(�������ӿ���ĸ���)��
(2)ʵ��ʱ���Կ���Ϊԭ���Ʊ�AlN��װ��A�л�ԭ���۵�����Ϊ________________��װ��B���Լ�XΪ_____________________��
(��)�ⶨ��Ʒ����
ȡm g�IJ�Ʒ��������װ�òⶨ��Ʒ��AlN�Ĵ���(�г�װ������ȥ)��
��֪��AlN + NaOH + H2O �� NaAlO2 + NH3��
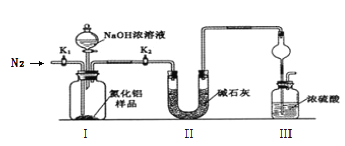
(3)�������ʵ�鲽�裺��װ��ʵ��װ�ã�����_________________________________������ʵ��ҩƷ����������ʵ������ǹر�______________________________����______________���ٴ�Һ©��������������NaOHŨ��Һ��رգ������ٲ������塣��______________��ͨ�뵪��һ��ʱ�䣬�ⶨװ��III��Ӧǰ��������仯Ϊn g��
(4)ʵ����������Ʒ��AlN�Ĵ���Ϊ___________��(�ú�m��n�Ĵ���ʽ��ʾ)��
(5)����ʵ��������Ȼ����ȱ�ݣ�����Ϊ���ܵ�ȱ�ݼ��ᵼ�µIJⶨ���____________(�� ��ƫ��������ƫ��������)���______________________________________________________��
���𰸡�fedcab(��ba)gh(��hg) ����O2 Ũ���� ���װ�õ������� K1 K2 �� K1 ![]() ƫ�� ��������ˮ�����²ⶨ���ƫ��
ƫ�� ��������ˮ�����²ⶨ���ƫ��
��������
��1��AlN�������ܻ���ˮ�⣬�������ڵ�����Χ��1700���ϳɡ���ô���������ȥˮ��O2����ԭ���۳�ȥO2��Bװ����X����Ϊ�˳�ȥˮ��Ӧ��ΪŨ���ᣬCװ�ó�ȥ�����е�CO2��Ӧ����Cװ�ó�ȥCO2������Aװ�ó�ȥO2������ȥˮ������D����Al��Ӧ������ü�ʯ����ֹ��������װ�ã������Ʒ���ʡ���Ϊfedcab(��ba)gh(��hg)��
��2����ԭ���۵����ó�ȥ�����������ʵ��������ţ�Bװ�õ�Ŀ���dz�ȥˮ��XΪŨ���ᣬ��Ϊ����O2 Ũ���
��3��ʵ�鲽�裬��װҩƷ֮ǰ��Ҫ��װ�ý��м�©��ʵ�鿪ʼ���У����Ȳ�ͨ�뵪����K1�ǹرյģ�K2�Ǵģ���Ӧ�����ٲ�������ʱ����Ӧֹͣ����Ҫ�����еİ���ͨ��Ũ�����б����գ������Ҫͨ�뵪������K1����Ϊ���װ�õ������� K1 K2 �� K1��
(4)���ݷ���ʽ
AlN ~ NH3
41 17
m(AlN) n
�ɵ�m(AlN)=![]() ��
��![]() ����Ϊ
����Ϊ![]() ��
��
��5��������Ӧ�м�����ˮ��������������ˮ��ʹ�ð������ܱ�Ũ������ȫ���գ�����������ƫС�����ƫ�͡���Ϊƫ�� ��������ˮ�����²ⶨ���ƫ�͡�


 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���ͭ�㷺Ӧ�����л��ϳɡ�ʯ�͡���֬��Ⱦ�ϵȹ�ҵ����ij��ͭ���(��Cu2S��CuS��FeS��)Ϊԭ����ȡCuCl�Ĺ�������������
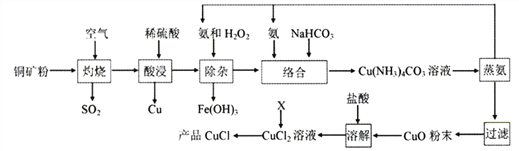
��֪����CuS��Cu2S��FeS���չ������ΪCu2O��FeO��
��Ksp(CuCl)=2��10-7��2Cu+=Cu+Cu2+��ƽ�ⳣ��K1=1��106
�ش�����������
��1����������ʱ������ԭ��Ԫ����____________(��Ԫ�ط���)��
��2�������������H2SO4���õ������98%H2SO4��ˮ��϶��ɡ�ʵ�������Ƹ�������Һ����IJ�������������������ͷ�ι���������_______���������ʱ����˹����ԭ����__________________��
��3�������������ܷ�Ӧ����ʽ��_____________________��
��4�����������Ӧ�е�NH3��NaHCO3���۱�ֵ��____________________��
��5���������������ڼ�ѹ�����½��е�ԭ����________________��
��6��X���Գ�����������еIJ�������X��SO2ʱ��ͨ��CuCl2��Һ�з�Ӧ�����ӷ���ʽ��________________����X��Cuʱ����ӦCu+Cu2++2Cl-=2CuCl��ƽ�ⳣ��K2=_________��
��7����ͭΪ�������NaCl��ҺҲ�ɵõ�CuCl��д�������缫��Ӧʽ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��G(���ǻ�������)�Ǻϳ�ij���Ƹ�Ѫѹҩ����м��塣һ���ɷ�����A�Ʊ�G�ĺϳ�·������ͼ��ʾ��

��ش��������⣺
(1)A������Ϊ___________��
(2)�Լ�M��___________��B��C�ķ�Ӧ������___________��
(3)E�Ľṹ��ʽΪ___________��F�к��й����ŵ�������___________��
(4)д��D��E��Ӧ�Ļ�ѧ����ʽ��___________��
(5)H��G��ͬ���칹�壬��������������������FeCl3��Һ������ɫ��Ӧ���ں˴Ź���������5��壬�����֮��Ϊ1�U2�U2�U2�U1����д��3������������H�Ľṹ��ʽ��___________��
(6)�����������Ⱦ�����塢���ϼ����ܼ��ȵ��������ο���Ŀ�е��й���Ϣ������ɱ��Ʊ�������ĺϳ�·��(���Լ���ѡ)��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C�����ֶ���������Ԫ�ء�����һ�ֳ������������壬A��B��Cԭ������֮��Ϊ26������֮�������ͼ��ʾ��ϵ������˵����ȷ����

A. ����̬�⻯����ȶ���:C > B
B. ԭ�Ӱ뾶��С: C > B > A
C. �����ͬԪ�ص���һ������ֻ���Ǽ��Լ�
D. ��ҵ�ϳ��õ����������������ȡA�ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤±�ص��������Ե����ǿ����ijС������ͼ��ʾװ�ý���ʵ�飨�г���������ȥ���������Ѽ��飩��B��C�о�����10mL 1mol/L��NaBr��Һ��

ʵ����̣�
��.���ɼУ�����a���μ�Ũ���ᡣ
��.��B��C�е���Һ����Ϊ��ɫʱ���н����ɼС�
��.��B����Һ�ɻ�ɫ��Ϊ����ɫʱ���رջ���a��
��.����b��������Һ�����D�У�ȡ���Թܲ���
��1����֤������������ǿ�ڵ��ʵ��������________________________________________��
��2��B����Һ������Ӧ�Ļ�ѧ����ʽ��____________________________________________��
��3�����̢��г��ֵ�������________���ɴ˿�֤�������Խ�ǿ����________���Br2����I2������
��4����ƹ��̢��Ŀ����__________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���ձ���ʢ�е������ˮ��ú�ͣ��ֽ�һС������Ƽ����ձ��У����ƶ��ܹ۲쵽��ʵ������Ӧ�ǣ� ��

A. ��������ú�Ͳ���
B. �ƾ�ֹ����Һ��֮��
C. �Ƴ���ˮ����
D. ������Һ����渽����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�־��и������ȵ����ɵ��ʾ��ͼ��ͼ��ʾ��ʯī�缫�������ĵ缫��ӦΪMnO2+e��+H2O=MnO(OH)+OH-����װ�ù���ʱ������������ȷ����

A. Al�缫���ĵ缫��Ӧʽ��A1-3e-+3NH3��H2O=Al(OH)3+3NH4+
B. ʯī�缫�ϵĵ��Ʊ�Al�缫�ϵĵ�
C. ÿ����27gAl����3mol����ͨ����Һת�Ƶ�ʯī�缫��
D. ������ʳ��ˮ+NaOH��Һ���������Һ���缫��Ӧʽ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��(NH4)2CO3(s)�TNH4HCO3(s)+NH3(g) ��H=+74.9kJ��mol��1������˵������ȷ����
A. �÷�Ӧ�����ȷ�Ӧ�����һ�������Է�����
B. �÷�Ӧ����������һ�������Է�����
C. �÷�Ӧ����S>0�����Ը��¿����Է�����
D. �Է����еķ�Ӧ�����Ƿ��ȷ�Ӧ�������Է����еķ�Ӧ�������ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��H2A���ᣩ��K1=4.3��10��7��K2=2.1��10��12��H2B���ᣩ��K1=1.0��10��7��K2=6.3��10��13������Ũ����ͬ��������Һ�������������������������������ش�л�����⣺
(1)��H+��Ũ�ȣ�H2A________H2B������Һ�ĵ���������H2A________H2B��
(2)д��H2B����Һ�����е�����__________��
(3)��д��H2A�ĵ��뷽��ʽ___________����д��NaHA�ĵ��뷽��ʽ__________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com