
����Ŀ����ҵ��һ����CO��H2Ϊԭ�Ϻϳɼ״����÷�Ӧ���Ȼ�ѧ����ʽΪ��
CO(g)+ 2H2(g)![]() CH3OH(g) ��H
CH3OH(g) ��H
��1����֪CO(g)��H2(g)�ı�ȼ���ȷֱ�Ϊ ��H=��283kJmol-1�� ��H=��286kJmol-1����CH3OH(g)+3/2O2(g) ![]() CO2(g)+2H2O(l) ��H=��761kJmol-1����CO(g)+ 2H2(g)
CO2(g)+2H2O(l) ��H=��761kJmol-1����CO(g)+ 2H2(g)![]() CH3OH(g)����H= ___________��
CH3OH(g)����H= ___________��
��2��Ϊ�����CO��H2�Ʊ��״�����Ч�ʺͲ�������ҵ������ͨ����ȡ�Ĵ�ʩ��___________________________________________����д�����㣩
��3��ʵ����ģ����CO��H2��Ӧ���Ƽ״�����250 ���£���һ������CO��H2Ͷ��10 L���ܱ������У������ʵ����ʵ���Ũ�ȣ�mol��L-1���仯���±���ʾ��
2 min | 4 min | 6 min | |
CO | 0.07 | 0.05 | 0.05 |
H2 | x | 0.10 | 0.10 |
CH3OH | 0.03 | 0.05 | 0.05 |
��250 ��ʱ���÷�Ӧ��ƽ�ⳣ��K=___________��
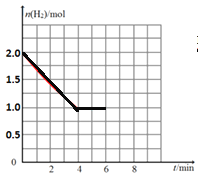
����ͼ1�л�����Ӧ��ʼ����6 minʱH2�����ʵ����ı仯���ߣ���������ʵ������ꡣ_______
��4�����õ��״�ˮ��Һ�Ʊ����������ŵ������Ҫ�ĵ�ѹ�ͣ�װ����ͼ2��д�� �����缫��Ӧ����ʽ____________________________________________________�������ܷ�Ӧ��ѧ����ʽ__________________________________________��
���𰸡���94 kJmol-1 ԭ��ѭ��ʹ�ã�ʹ�ô�������ʱ���״�Һ�����룬���ƺ����¶ȣ���ѹ 100 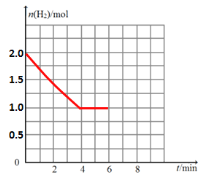 CH3OH��6e��+ H2O= CO2��+6 H+ CH3OH+ H2O
CH3OH��6e��+ H2O= CO2��+6 H+ CH3OH+ H2O![]() CO2��+3H2��
CO2��+3H2��
��������
��1����֪CO(g)��H2(g)�ı�ȼ���ȷֱ�Ϊ ��H=��283kJmol-1�� ��H=��286kJmol-1�����CO(g)+ 1/2O2(g)= CO2(g) ��H=��283kJmol-1����H2(g)+ 1/2O2(g)= H2O(l) ��H=��286kJmol-1��CH3OH(g)+3/2O2(g) ![]() CO2(g)+2H2O(l) ��H=��761kJmol-1����+��
CO2(g)+2H2O(l) ��H=��761kJmol-1����+��![]() 2-�ۣ�CO(g)+ 2H2(g)
2-�ۣ�CO(g)+ 2H2(g)![]() CH3OH(g)����H=��94 kJmol-1���𰸣���94 kJmol-1��
CH3OH(g)����H=��94 kJmol-1���𰸣���94 kJmol-1��
��2����CO(g)+ 2H2(g)![]() CH3OH(g)����H=��94 kJmol-1��֪���CO��H2�Ʊ��״�����Ч�ʺͲ�������Ҫ��ȡ�Ĵ�ʩ�ǣ�ԭ��ѭ��ʹ�ã�ʹ�ô�������ʱ���״�Һ�����룬���ƺ����¶ȣ���ѹ���𰸣�ԭ��ѭ��ʹ�ã�ʹ�ô�������ʱ���״�Һ�����룬���ƺ����¶ȣ���ѹ��
CH3OH(g)����H=��94 kJmol-1��֪���CO��H2�Ʊ��״�����Ч�ʺͲ�������Ҫ��ȡ�Ĵ�ʩ�ǣ�ԭ��ѭ��ʹ�ã�ʹ�ô�������ʱ���״�Һ�����룬���ƺ����¶ȣ���ѹ���𰸣�ԭ��ѭ��ʹ�ã�ʹ�ô�������ʱ���״�Һ�����룬���ƺ����¶ȣ���ѹ��
��3��������ͼ����֪4minʱCO(g)+ 2H2(g)![]() CH3OH(g)��Ӧ�ﵽƽ�⣬��ʱ�����ʵ�Ũ��Ϊ��c(CO)= 0.05 mol��L-1, c(H2)= 0.10 mol��L-1, c(CH3OH )=0.05 mol��L-1,���Ը÷�Ӧ��ƽ�ⳣ��K= c(CH3OH )/ c(CO)
CH3OH(g)��Ӧ�ﵽƽ�⣬��ʱ�����ʵ�Ũ��Ϊ��c(CO)= 0.05 mol��L-1, c(H2)= 0.10 mol��L-1, c(CH3OH )=0.05 mol��L-1,���Ը÷�Ӧ��ƽ�ⳣ��K= c(CH3OH )/ c(CO)![]() c2(H2)= 0.05/0.05
c2(H2)= 0.05/0.05![]() 0.10)2=100��
0.10)2=100��
�� CO(g) + 2H2(g)![]() CH3OH(g)
CH3OH(g)
��ʼŨ�ȣ�mol��L-1�� x y 0
�仯Ũ�ȣ�mol��L-1�� 0.05 0.10 0.05
ƽ��Ũ�ȣ�mol��L-1�� 0.05 0.10 0.05
����x=0.10 mol��L-1, y=0.20 mol��L-1��c(H2)��ʼ=0.20 mol��L-1��ƽ��Ũ��Ϊc(H2)ƽ��=0.10 mol��L-1����Ӧ��ʼ����6 minʱH2�����ʵ����ı仯����Ϊ
 ��
��
��4�����õ��״�ˮ��Һ��װ��ͼ ��CH3OH![]() CO2֪CԪ�صĻ��ϼ����ߣ�ʧ���ӣ����������������缫��Ӧ����ʽΪ��CH3OH��6e��+ H2O= CO2��+6 H+ ��������H2O
CO2֪CԪ�صĻ��ϼ����ߣ�ʧ���ӣ����������������缫��Ӧ����ʽΪ��CH3OH��6e��+ H2O= CO2��+6 H+ ��������H2O![]() H2�����˻�ԭ��Ӧ�����Ե����ܷ�Ӧ��ѧ����ʽCH3OH+H2O
H2�����˻�ԭ��Ӧ�����Ե����ܷ�Ӧ��ѧ����ʽCH3OH+H2O![]() CO2��+3H2�����𰸣�CH3OH��6e��+ H2O= CO2��+6 H+��CH3OH+ H2O
CO2��+3H2�����𰸣�CH3OH��6e��+ H2O= CO2��+6 H+��CH3OH+ H2O![]() CO2��+3H2����
CO2��+3H2����
��


 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ�����������ʵ�������ȷ����(����)
ѡ�� | ʵ�� | ���� | ʵ����� |
A | ��ij��Һ���ȵμ�����ϡ���ᣬ�ٵμ�����BaCl2��Һ | ���ְ�ɫ���� | ԭ��Һ�к���SO42-��SO32-��HSO3-�е�һ�ֻ��� |
B | ��װ��Fe(NO3)2��Һ���Թ��м���ϡ���� | �ڹܿڹ۲쵽����ɫ���� | HNO3�ֽ����NO2 |
C |
| ��������Ϊ��ɫ���ұ������Ϊ��ɫ | �����ԣ�Cl2>Br2>I2 |
D | SO2��SO3�������ͨ��Ba(NO3)2��Һ | ���ְ�ɫ���� | �õ��ij���ֻ��BaSO4 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA(g)��B(g) ![]() C(g)��D(g)�����������仯��ͼ������˵����ȷ���ǣ� ��
C(g)��D(g)�����������仯��ͼ������˵����ȷ���ǣ� ��

A. �÷�ӦΪ���ȷ�Ӧ
B. �����¶ȣ�����A��ת��������
C. �������ʱ�����Խ��ͷ�Ӧ��
D. ����ѹǿ���ܹ����̷�Ӧ�ﵽƽ��״̬��ʱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ���ۺ�����һֱ���о����⡣ij����Ȼ��ˮ(��Ҫ��Na����K����Ca2����Mg2����Cl����SO42����Br����CO32����HCO3��������)���о��ú�ˮ����ȼú�ŷŵĺ���SO2�����Ĺ���������ͼ��ʾ������˵������ȷ����
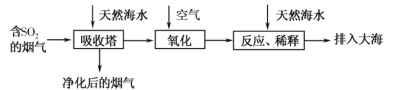
A.��������Ȼ��ˮ������
B.���������п��ܷ��������ӷ�ӦΪ2SO2��2H2O��O2=4H����2SO42��
C.�������Һ����Ȼ��ˮ��ȣ�ֻ��SO42�����������˱仯
D.�����������Һ����������ᾧ���õ��ľ�����CaSO4�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڲ�ͬ�¶��£�ˮ��Һ��c(H��)��c(OH��)��ϵ��ͼ��ʾ������˵������ȷ����
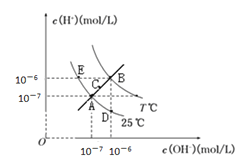
A. ͼ�����Kw��Ĺ�ϵ��B>C>A=D=E
B. ���¶Ȳ����ˮ�У�����������NH4Cl����ʵ�ִ�A��䵽C��
C. D���Ӧ��ˮ��Һ�У�������NH4+��Fe3+��Cl����NO3������ͬʱ����
D. ������B��ʱ����pH =2��������Һ�� pH = 10��KOH��Һ�������ϣ�������Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������п��Ϊ��пҩ�����м�Ч�졢�����ʸߡ�������С��ʹ�÷�����ŵ㡣ijѧϰС����ʵ�����������Ǻ�����пΪ��Ҫԭ�Ϻϳɸ����ʡ�
��Ӧԭ����CH2OH(CHOH)4CHO + H2O2 ![]() CH2OH(CHOH)4COOH + H2O
CH2OH(CHOH)4COOH + H2O
2CH2OH(CHOH)4COOH + ZnO ![]() Zn[CH2OH(CHOH)4COO] 2 + H2O
Zn[CH2OH(CHOH)4COO] 2 + H2O
��Ƶĺϳ�·��Ϊ��
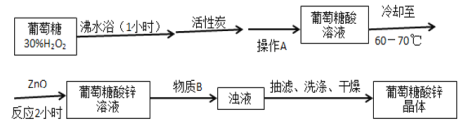
�����Ϣ���£�
��������п������ˮ�����Ҵ���ˮ�Ļ���ܼ��е��ܽ�����Ҵ���������ı仯����ʾ��ͼ��ͼ1
ʵ�������漰�IJ���װ����ͼ��ʾ��ͼ2װ�����Ʊ��������ᣬ����ZnO��Ӧ�Ʊ�
��������п����ͼ3Ϊ����װ��
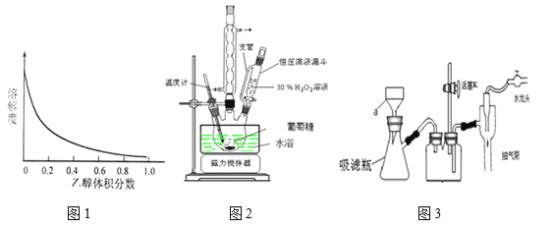
�����������Ϣ���ش��������⣺
��1��ͼ2�к�ѹ��Һ©����֧�ܵ�������___________��ͼ3��aװ�õ�����____________��
��2��30%H2O2���õ����ʵ�������������ǵ�3�������Ҳ�δһ�����������ǻ�ϣ��������ú�ѹ��Һ©�������μӵ�����_________________________________��
��3������A��______________������B��________________��
��4��������ϻ���;ֹͣ����ʱ��Ӧ��___________________��Ȼ��____________________��
��5��������ƿ�е���������п����ת�뵽����װ����ʱ��ƿ����������ճ���������壬��ѡ��Һ�彫ƿ���ϵľ����ϴ������ת�뵽����װ���У�����Һ������ʵ���_______��
A ��ˮ�Ҵ� B ����NaCl��Һ C 70���Ҵ�ˮ��Һ D ��Һ
��6������˵����ȷ����________��
A ��������Һ�����30%H2O2��������ת����������ᣬ�Ⱦ����ַ���
B ZnO��ĩ���������ᷴӦʱ�����ô��������������ZnO��ĩ����������ĽӴ�������ӿ췴Ӧ����
C �ڳ��˹����У��������ƿ�е�Һ���ӽ�֧�ܿ�ʱ����ε�����ƿ�ϵ���Ƥ�ܣ���������ƿ��֧�ܿڵ�����Һ
D ����������п������ڸ������п��Է������ڸ������з��и����������������ˮCoCl2��ָʾ�Ƿ�ø�������������CoCl2Ϊ��ɫ��˵��������Ѿ�ʧЧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2����Ư�۵Ⱥ������������Լ��ٶ������Σ������ClO2���״�������䣬��˽����Ƴ��������ơ�
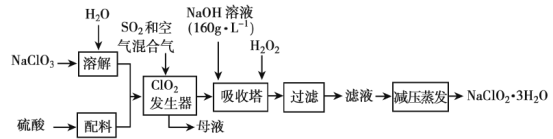
��֪����NaClO2���ܽ�����¶����߶������¶ȹ����ֽ⣬�ʵ������¿ɽᾧ����NaClO2��3H2O��
�ڴ�ClO2�ֽⱬը��һ����ϡ����������ϡ�͵�10�����½ϰ�ȫ��
��1���ڷ������й�����������ÿ�����___(�����)��
A��SO2������SO3����ǿ����
Bϡ��ClO2�Է�ֹ��ը
C��NaClO3������ClO2
��2�������ClO2����������Ӧ���ʵĴ�ʩ��___��
��3���������ڷ�Ӧ�����ӷ���ʽΪ___��
��4����ȡ����ѹ����������������ѹ��������ԭ����___��
��5���ⶨ�ֲ�Ʒ���������Ƶĺ�����ʵ�����£�
a.ȷ��ȡ��������������Ʒmg��С�ձ��У�������������ˮ�����ĵ⻯�ؾ��壬�ٵ���������ϡ���ᣬ��ַ�Ӧ�������û��Һ���250 mL������Һ��(��֪��ClO2����4I����4H����2H2O��2I2��Cl��)
b.��ȡ25.00mL������Һ����ƿ�У��Ӽ��ε�����Һ����c mol��L��1Na2S2O3��Һ�ζ����յ㣬�ظ�2�Σ����ƽ��ֵΪV mL��(��֪��I2��2S2O32����2I����S4O62��)
�ٴﵽ�ζ��յ�ʱ������Ϊ___��
�ڸ���Ʒ��NaClO2����������Ϊ___(�ú�m��c��V�Ĵ���ʽ��ʾ������軯��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�������йط�Ӧ������������ǣ� ��
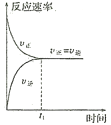
A.��ʼ��Ӧʱ������Ӧ��������淴Ӧ����Ϊ��
B.���ŷ�Ӧ�Ľ��У�����Ӧ������С���淴Ӧ����������
C.��Ӧ����![]() ʱ������Ӧ�������淴Ӧ������ȣ���Ӧֹͣ
ʱ������Ӧ�������淴Ӧ������ȣ���Ӧֹͣ
D.��Ӧ��![]() ֮������Ӧ�������淴Ӧ������ȣ���Ӧ�ﵽ��ѧƽ��״̬
֮������Ӧ�������淴Ӧ������ȣ���Ӧ�ﵽ��ѧƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10 mol H2��5 mol N2����10 L����ܱ������ڣ�һ���¶��·������·�Ӧ��3H2(g)+N2(g) ![]() 2NH3(g)���������0.2 s�ڣ�����H2��ƽ������Ϊ0.06 mol��L1��s1������0.2 sĩ��������NH3�����ʵ�����
2NH3(g)���������0.2 s�ڣ�����H2��ƽ������Ϊ0.06 mol��L1��s1������0.2 sĩ��������NH3�����ʵ�����
A. 0.12 molB. 0.08 molC. 0.04 molD. 0.8 mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com