
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或 最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
| A. | 元素②⑥形成的化合物具有两性 | |
| B. | 元素②气态氢化物的沸点小于元素⑤气态氢化物的沸点 | |
| C. | 元素⑤对应的离子半径大于元素⑦对应的离子半径 | |
| D. | 元素④的最高价氧化物的水化物比元素⑤的最高价氧化物的水化物酸性强 |
分析 ②⑤的最低价都为-2价,应该为ⅥA族元素,根据原子半径可知②为O元素、⑤为S元素;①⑦⑧的最高正化合价为+1价,结合原子半径大小可知:①为H元素、⑦为Li元素、⑧为Na元素;③⑥的最高价为+3价,结合原子半径可知:③为B元素、⑥为Al元素;④的最低价为-1价,为ⅤⅡA族元素,其原子半径大于②O元素,则④为Cl元素,据此结合元素周期律知识进行解答.
解答 解:②⑤的最低价都为-2价,应该为ⅥA族元素,根据原子半径可知②为O元素、⑤为S元素;①⑦⑧的最高正化合价为+1价,结合原子半径大小可知:①为H元素、⑦为Li元素、⑧为Na元素;③⑥的最高价为+3价,结合原子半径可知:③为B元素、⑥为Al元素;④的最低价为-1价,为ⅤⅡA族元素,其原子半径大于②O元素,则④为Cl元素,
A.元素②⑥形成的化合物为氧化铝,氧化铝为两性氧化物,故A正确;
B.元素②气态氢化物为水,元素⑤气态氢化物为硫化氢,由于水分子中存在氢键,则水的沸点大于硫化氢,故B错误;
C.元素⑤对应的离子为硫离子,元素⑦对应的离子为锂离子,硫离子含有3个电子层、锂离子含有1个电子层,所以硫离子的离子半径大于锂离子,故C正确;
D.元素④的最高价氧化物的水化物高氯酸,元素⑤的最高价氧化物的水化物为硫酸,由于非金属性:Cl>S,则高氯酸的酸性大于硫酸,故D正确;
故选B.
点评 本题考查了元素周期表和元素周期律的综合应用,题目难度中等,根据表中数据正确判断各元素名称为解答关键,注意熟练掌握元素周期表结构、元素周期律的内容,B为易错点,注意水中存在氢键,导致其沸点较高.


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 与Al反应放出H2的溶液:Mg2+、Ca2+、HCO3-、NO3- | |
| B. | 10mol•L-1的浓氨水:Al3+、NH4+、NO3-、I- | |
| C. | 0.1mol•L-1KMnO4溶液:Na+、Fe2+、SO42-、Cl- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液K+、Na+、AlO2-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
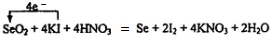 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
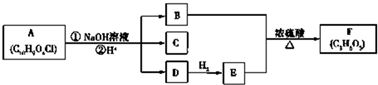
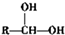 $\stackrel{自动脱水}{→}$
$\stackrel{自动脱水}{→}$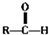 (R为羟基)
(R为羟基) .
. .
.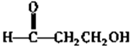 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
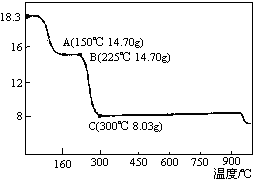 草酸钴是制备钴的氧化物的重要原料.如图为二水合草酸钴(CoC2O4•2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物.
草酸钴是制备钴的氧化物的重要原料.如图为二水合草酸钴(CoC2O4•2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
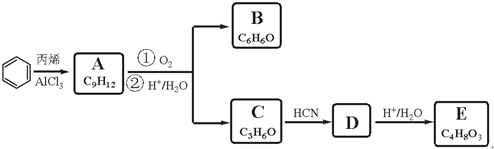
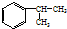 ,A的含有苯环的同分异构体(除A外)有7种.
,A的含有苯环的同分异构体(除A外)有7种.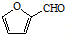 )是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂,写出该反应的化学方程式
)是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂,写出该反应的化学方程式 .
. G:
G: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| B. | 钢铁表面烤蓝生成一层致密的Fe3O4,能起到防腐蚀作用 | |
| C. | 积极开发新能源,如可燃冰、生物汽油等,减少对化石燃料的依赖 | |
| D. | 随着化学的发展,化学实验方法并不是化学研究的唯一手段 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

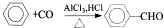
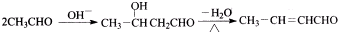
 .
.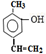 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通常状况下,NO2是无色的气体 | |
| B. | SO2能漂白品红等物质,说明SO2有氧化性 | |
| C. | 加热时,铁单质与浓硝酸不发生反应 | |
| D. | 二氧化氯具有强氧化性,可用于自来水的杀菌消毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com