
3molA和2.5molB混合于容积为2L的容器内,使它们发生反应2A(s)+3B(g) 2C(g)+D(g),经过5min生成0.5molD,下列说法正确的是
2C(g)+D(g),经过5min生成0.5molD,下列说法正确的是
A.B的平均消耗速率为0.3mol/(L min)
min)
B. C的平衡浓度为2mol/L
C.平衡后,增大压强,平衡将向正方向移动
D.若反应容器内气体的密度不再发生变化,说明反应已经达到平衡
【答案】D
【解析】
试题分析:A、参加反应的B为1.5mol,浓度是1.5mol÷2L=0.75mol/L,则v(B)=0.75mol/L÷5min=0.15mol/(L•min),故A不正确;B、起始时充入3molA和2.5molB混合气体;经过5min生成0.5molD
2A(s)+3B(g) 2C(g)+D(g)
2C(g)+D(g)
起始量(mol) 3 2.5 0 0
变化量(mol) 1 1.5 1 0.5
平衡量(mol) 2 1 1 0.5
c(C)=0.5mol/L,故B错误;
C、正方应是体积不变的可逆反应,则平衡后,增大压强,平衡不移动,故C错误;D、密度是气体质量与容器容积的比值,容器容积不变,但气体的质量变化,所以若反应容器内气体的密度不再发生变化,说明反应已经达到平衡,故D正确,答案选A。
考点:考查化学平衡的基本计算方法,速率计算的应用,平衡状态的判断,影响平衡的因素


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
反应4NH3+5O2  4NO+6H2O在一定体积的密闭容器中进行,30 s后NO的物质的量浓度增加了3 mol/L,则下列反应速率正确的是
4NO+6H2O在一定体积的密闭容器中进行,30 s后NO的物质的量浓度增加了3 mol/L,则下列反应速率正确的是
A.v (NO)=0.02 mol·(L·s)-1 B.v (NO)=0.2mol·(L·s)-1
C.v (NH3)=0.01 mol·(L·s)-1 D.v (NH3)=0.1 mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
分类是化学学习与研究的常用方法,下列分类正确的是
A.Na2O2、MgO、Al2O3均属于碱性氧化物
B.纯碱、烧碱、熟石灰均属于碱
C.酸、碱、盐之间发生的反应均属于复分解反应
D.混合物、分散系、胶体从属关系如图所示
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH  B.分别在两种溶液中滴加甲基橙
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别 D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:________________________ 。
(4) Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________(填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
用铝制易拉罐收集满CO2,快速加入过量NaOH浓溶液,立即把口封闭。发现易拉罐“咔咔”作响,并变瘪了:过一会儿,易拉罐又会作响并鼓起来。下列说法正确的是
A.导致易拉罐变瘪的离子反应是:CO2+OH-═HCO3-
B.导致易拉罐又鼓起来的反应是: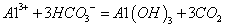
C.若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象
D.上述过程中与NaOH溶液反应的物质有三种,且反应结束后的溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的叙述中,合理的是__________
A实验室中少量金属钠、钾保存在汽油中
B容量瓶、分液漏斗、酸(碱)式滴定管等仪器在使用前都必须检验是否漏水
C圆底烧瓶、锥形瓶、烧杯加热时都应垫在石棉网上
D用一定浓度的盐酸滴定未知浓度的氢氧化钠溶液时,酸式滴定管记录起始体积时,平视读数,终点时俯视,所测碱的浓度偏高
E.不用其它化学试剂即可鉴别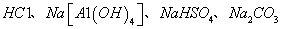 四种无色溶液
四种无色溶液
F.可以用渗析的方法除去淀粉溶液中的氯化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
T ℃下的溶液中,c(H+)=1.0×10-xmol·L-1,c(OH-)=1.0×10-ymol·L-1,x与y的关系如图所示。下列说法不正确的是( )
 A.T ℃时,水的离子积Kw为1×10-13
A.T ℃时,水的离子积Kw为1×10-13
B.T>25
C.T ℃时,pH=7的溶液显碱性
D.T ℃时,pH=12的苛性钠溶液与pH=1的稀硫酸等体积混合,溶液的pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
以下物质间的转化通过一步反应不能实现的是 ( )
A.HCl →Cl2→HClO→NaClO B.Na→Na2O2→Na2CO3→NaHCO3
C.Si→SiO2→H2SiO3→Na2SiO3 D.Al→NaAlO2 →Al(OH)3→Al2O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com