

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀pH(离子初始浓度0.01 mol/L) | 4 | 2.3 | 10.4 |
| 完全沉淀pH(离子浓度<10-5mol/L) | 5.2 | 4.1 | 12.4 |
科目:高中化学 来源:不详 题型:单选题
A.浊液a中存在沉淀溶解平衡:Mg (OH) 2(s) Mg2+(aq)+2OH-(aq) Mg2+(aq)+2OH-(aq) |
| B.滤液b中不含有Mg2+ |
| C.②中颜色变化说明Mg (OH)2转化为Fe(OH)3 |
| D.实验可以证明Fe(OH)3比Mg (OH)2更难溶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
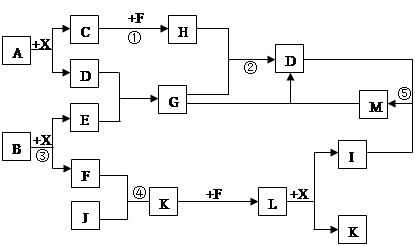
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①⑥⑤③ | B.②③④③ | C.②③⑤③ | D.①③⑤③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第二周期ⅣA族 | B.第三周期ⅡA族 |
| C.第二周期ⅥA族 | D.第三周期ⅣA族 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
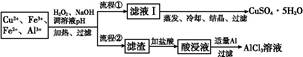
| 离子 | Fe3+ | Fe2+ | Al3+ | Cu2+ |
| pH范围 | 2.2~3.2 | 5.5~9.0 | 4.1~5.0 | 5.3~6.6 |
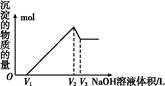
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com