


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、通常用小黑点来表示电子的多少,黑点密度大,电子数目大 |
| B、通常用小黑点来表示电子绕核作高速圆周运动 |
| C、黑点密度大,单位体积内电子出现的机会大 |
| D、电子云图是对运动无规律性的描述 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2(g)+O2(g)═2H2O(l);△H1 | ||
B、C(s)+
| ||
| C、CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H3 | ||
| D、C(s)+O2(g)═CO2(g);△H4 | ||
| E、C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(g);△H5 | ||
| F、NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H6 | ||
| G、2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l);△H7 | ||
| H、CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 中带*的C原子.若同一个碳原子上连着2个碳碳双键(如C=C=C)时,分子极不稳定,不存在.某链烃C7H10的众多同分异构体中:
中带*的C原子.若同一个碳原子上连着2个碳碳双键(如C=C=C)时,分子极不稳定,不存在.某链烃C7H10的众多同分异构体中: 、
、
 3种外,还有
3种外,还有查看答案和解析>>
科目:高中化学 来源: 题型:
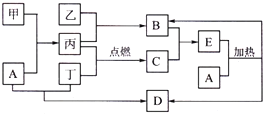
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界存在大量的单质硅 |
| B、SiO2与任何酸都不起反应 |
| C、光导纤维被广泛应用于能量传输和信息传输 |
| D、SiO2的化学性质活泼,能与多种物质发生化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界中存在大量的单质硅 |
| B、石英、水晶、玛瑙的主要成分都是二氧化硅 |
| C、二氧化硅的化学性质活泼,能跟酸、碱发生化学反应 |
| D、自然界中二氧化硅都存在于石英矿中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com