

分析 题中能发生连续氧化的单质A,对应的D为强酸,则对应的反应有硫和氮元素的转化:C是红棕色的气体,则C为NO2,A在常温下为气体,则A应为N2,氮气与氧气发生反应生成B为NO,一氧化氮氧化成二氧化氮,二氧化氮与水反应D为HNO3,结合物质的性质解答该题.
解答 解:题中能发生连续氧化的单质A,对应的D为强酸,则对应的反应有硫和氮元素的转化:C是红棕色的气体,则C为NO2,A在常温下为气体,则A应为N2,氮气与氧气发生反应生成B为NO,一氧化氮氧化成二氧化氮,二氧化氮与水反应D为HNO3,浓硝酸与铜反应生成二氧化氮,反应的化学方程式为Cu+4 HNO3(浓)═Cu(NO3)2+2 NO2↑+2 H2O,
故答案为:Cu+4 HNO3(浓)═Cu(NO3)2+2 NO2↑+2 H2O.
点评 本题考查无机物的推断,题目难度不大,本题注意根据物质的颜色以及连续发生氧化反应的特征为突破口进行推断.


科目:高中化学 来源: 题型:选择题
| A. | 苯丙醇胺的结构简式为: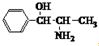 ,其分子中有2个手性碳原子 ,其分子中有2个手性碳原子 | |
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| C. | 完全由非金属元素形成的化合物中也可能含有离子键 | |
| D. | CO2、SiO2都是分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
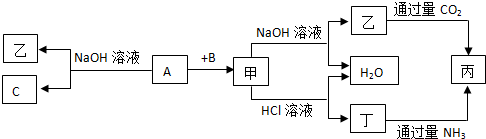
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应中能量变化的大小与反应物的多少无关 | |
| B. | 化学反应必然伴随能量的变化 | |
| C. | 化学反应中能量的主要是由化学键变化引起的 | |
| D. | 能量变化是化学反应的基本特征之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水鉴别炭粉和二氧化锰 | |
| B. | 用闻气味的方法鉴别白酒和白醋 | |
| C. | 用澄清石灰水鉴别氮气和二氧化碳 | |
| D. | 用相互刻画的方法鉴别黄铜片和铜片 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com