
| A、溶液中c(H+)和c(OH-)都减小 |
| B、溶液中c(H+)增大 |
| C、醋酸电离平衡向右移动 |
| D、溶液的pH不变 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| ||
| ||
| A、两个反应都是置换反应 |
| B、反应②是吸热反应 |
| C、两个反应互为可逆反应 |
| D、两个反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L 1mol?L-1的NaClO溶液中含ClO-的数目为NA |
| B、78 g 苯含有碳碳双键的数目为3NA |
| C、常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA |
| D、标准状况下,2.24L Cl2与水充分反应转移的电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入KSCN溶液和盐酸,溶液变红色 | 原溶液一定含Fe3+ |
| B | 向某溶液中加入稀盐酸,产生使澄清石灰水变浑浊的无色无味气体 | 原溶液一定含CO32- |
| C | 向某溶液中加入稀盐酸无现象,再滴加BaCl2有白色沉淀 | 原溶液一定含SO42- |
| D | 向某溶液滴加稀NaOH溶液时,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 原溶液一定不含NH4+ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A、③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大 |
| B、分别加水稀释10倍,四种溶液的pH①>②>④>③ |
| C、①④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、VaL②与VbL③溶液混合后,若混合后溶液pH=7,则Va>Vb |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | C-H | Cl-Cl | C-Cl | H-Cl |
| 键能/kJ?mol-1 | X | 243 | 330 | 432 |
查看答案和解析>>
科目:高中化学 来源: 题型:
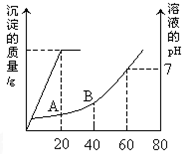 (1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=
(1)某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=查看答案和解析>>
科目:高中化学 来源: 题型:
 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com