
下列有关离子的检验方法及现象叙述正确的是( )
A.检验H+:向溶液中滴加石蕊试液,溶液变成蓝色,则证明溶液中含有H+
B.检验Cl-:先加入硝酸银溶液,生成白色沉淀,再加入稀硝酸,若沉淀不溶解,则证明含有Cl-
C.检验Fe2+:加入NaOH溶液,产生红褐色沉淀,则证明含有Fe2+
D.检验Fe3+:加入KSCN溶液,生成红色沉淀,则证明含有Fe3+
科目:高中化学 来源: 题型:
右图为硬脂酸甘油酯在碱性条件下水解的装置图。进行皂化反应时的步骤如下:
(1)在圆底烧瓶中加入8 g硬脂酸甘油酯,然后加入2 g氢氧化钠、5 mL水和10 mL酒精,加入酒精的作用是_____________________________________。
(2)隔着石棉网给反应物加热约10分钟,皂化反应基本完成,所得的
混合物为________(填“悬浊液”、“乳浊液”、“溶液”或“胶体”)。
(3)向所得混合物中加入________,静置一段时间后,溶液分为上下两层,肥皂在________层,这个操作称为________。
(4)图中长玻璃导管的作用为________。
(5)日常生活中用加热的纯碱溶液来洗涤粘有油脂的器皿的原因是__________________________________________________________________
________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中要测定部分变质的过氧化钠的纯度,可用如图装置实现。
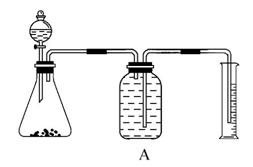
(1)锥形瓶中应放药品________,分液漏斗中放__________,锥形瓶中发生的化学方程式为_________________________________________。
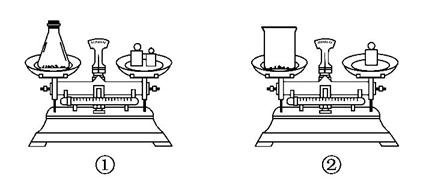
(2)如图用托盘天平称取样品,应选用如图中的__________(填“①”或“②”)。不选用另一装置的原因是___________________________________。
(3)若取用样品的质量为2.5 g,收集到气体的体积为280 mL(标准状况),则样品中Na2O2的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是
( )
A.3Br2+6KOH====5KBr+KBrO3+3H2O
B.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
C.2KNO3 2KNO2+O2↑
2KNO2+O2↑
D.NH4NO3 N2O↑+2H2O
N2O↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应中,水可以作氧化剂,作还原剂,既作氧化剂又作还原剂,既不作氧化剂又不作还原剂。下列反应与Br2+SO2+2H2O====H2SO4+2HBr相比较,水的作用不相同的是( )
A.Cl2+H2O HCl+HClO B.2F2+2H2O====4HF+O2
HCl+HClO B.2F2+2H2O====4HF+O2
C.2Na2O2+2H2O====4NaOH+O2↑ D.4Fe(OH)2+O2+2H2O====4Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学通过系统实验探究铝及其化合物的性质,操作正确且能达到目的的是 ( )
A.用互相滴加的方法可鉴别氯化铝溶液、氢氧化钠溶液
B.向氯化铝溶液中滴加过量氨水,最终得到澄清溶液
C.常温下铝与浓硝酸反应制得大量的NO2
D.AlCl3溶液加热蒸干得到无水氯化铝晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表是指导化学学习的重要工具。下图为元素周期表的一部分。请按要求填空。

(1)N在元素周期表中的位置是_____;N和F处于同一行,是由于它们的_________相同。
(2)以上元素中,原子半径最小的是_____(写元素符号);最高价氧化物对应水化物中酸性最强的是__________(写化学式)。
(3)Mg和Al中,金属性较强的是_______(写元素符号),写出一条能说明该结论的事实____________________。
(4)S和Cl中,非金属性较强的是_____(写元素符号),不能说明该结论的事实是_____。
a.氯气与铁反应生成FeCl3,硫与铁反应生成FeS
b.把Cl2通入H2S溶液中能发生置换反应
c.受热时H2S易分解,HCl不易分解
d.单质硫是固体,氯的单质是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
某市拟投资建设一个工业酒精厂,目的是用工业酒精与汽油混合制成“乙醇汽油”,以节省石油资源。已知制酒精的方法有三种:
①在催化剂作用下乙烯与水反应;
②CH3CH2Br+H2O―→CH3CH2OH+HBr
③(C6H10O5)n(淀粉)+nH2O酸或酶,nC6H12O6(葡萄糖),C6H12O6酒化酶,2C2H5OH+2CO2↑。
(1)方法①的化学反应方程式______________________________________。
(2)方法②的化学反应类型是_______________________________________。
(3)为缓解石油短缺带来的能源危机,你认为该市应选用哪一种方法生产工业酒精?__________。请简述理由_________________________________。
(4)如果从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的一组方法是__________。
A.① B.③
C.①③ D.①②③
(5)乙醇分子中的氧原子被硫原子取代后的有机物叫乙硫醇,其性质与乙醇相似,但乙硫醇有酸性,它能与NaOH等强碱溶液反应生成无色溶液。石油中因含乙硫醇(无色液体,微溶于水)使汽油有臭味且其燃烧产生的二氧化硫会污染环境,因此要把它除去。
①用化学方法除去石油样品中的乙硫醇,请写出有关反应的化学方程式_________________________________________________________________
________________________________________________________________。
②乙硫醇与乙酸在一定条件下可发生酯化反应,写出该反应的化学方程式_________________________________________________________________
_______________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com