
分析 根据M=$\frac{m}{n}$计算出该有机物的摩尔质量;根据C、H、O元素的质量分数计算出该有机物的最简式,据此可计算出该有机物的分子式.
解答 解:该有机物中各元素的质量分数为:C(40%)、H(6.67%)、O(53.33%),则该有机物分子中C、H、O原子数之比为:$\frac{40%}{12}$:$\frac{6.67%}{1}$:$\frac{53.33%}{16}$=1:2:1,
则该有机物的最简式为CH2O,
若0.2mol该物质的质量为36g,则该有机物的摩尔质量为:$\frac{36g}{0.2mol}$=180g/mol,则该有机物的相对分子量为18,
设该有机物分子式为(CH2O)n,则:30n=180,解得:n=6,
所以该有机物的分子式为:C6H12O6,
故答案为:C6H12O6.
点评 本题考查了有机物分子式的确定,题目难度中等,明确相对分子量与摩尔质量的关系为解答关键,注意掌握质量守恒定律、最简式法在确定有机物分子式中的应用,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
| 氧化剂 | I2的物质的量(mol) | 氧化剂 | I2的物质的量(mol) |
| H2O2 | IO3- | ||
| MnO4- | HNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
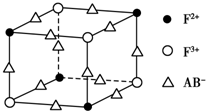 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素.A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子.
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素.A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁在氧气中燃烧 | |
| B. | 氢氧化钡晶体[Ba(OH)2•8H2O]与氯化铵晶体混合 | |
| C. | 锌与稀硫酸反应 | |
| D. | 氢氧化钡溶液与硫酸氢钠溶液混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清溶液中:AlO2-、SO42-、Na+、HCO3- | |
| B. | 在由水电离出的c(OH-)=10-13 mol•L-1的溶液中:I-、K+、Cl-、Ba2+ | |
| C. | 滴加甲基橙显红色的溶液:Fe2+、NH4+、SO42-、NO3- | |
| D. | c(H+)=c(OH-)的溶液:Fe3+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | $\frac{Vd}{MV+22400}$ | B. | $\frac{1000Vd}{MV+22400}$ | C. | $\frac{1000VdM}{MV+22400}$ | D. | $\frac{MV}{22.4(V+1)d}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 200 | 300 | 400 |
| 气体体积/Ml | 224 | 280 | 280 |
| 剩余固体/mg | 14 | 67.5 | 167.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | 以石墨作电极电解氯化铝溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| C. | AlCl3溶液中加入过量的浓氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 等体积、等浓度的稀溶液Ba(OH)2与NH4HCO3稀溶液混合:Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3•H2O+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚与溴水常温可以反应,而苯与溴水不能反应 | |
| B. | 乙烯能发生加成反应,而乙烷不能发生加成反应 | |
| C. | 苯酚与氢氧化钠溶液可以反应,而乙醇不能与氢氧化钠溶液发生反应 | |
| D. | 甲苯能使酸性高锰酸钾溶液褪色,而乙烷不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com