
”¾ĢāÄæ”æ¼ČæÉŅŌÓĆĄ“¼ų±šŅŅĶéŗĶŅŅĻ©£¬ÓÖæÉŅŌÓĆĄ“³żČ„ŅŅĶéÖŠ»ģÓŠµÄŅŅĻ©µÄ·½·ØŹĒ£Ø £©
A.ŌŚŅ»¶ØĢõ¼žĻĀĶØČėH2B.ĶØČė×ćĮæĖįŠŌøßĆĢĖį¼ŲČÜŅŗÖŠ
C.ĶØČė×ćĮæäåĖ®ÖŠD.·Ö±š½ųŠŠČ¼ÉÕ
”¾“š°ø”æC
”¾½āĪö”æ
A”¢ŅŅĶéŗĶŅŅĻ©ĶØČėĒāĘų£¬Ć»ĻÖĻ󣬲»ÄÜÓĆĄ“¼ų±šŅŅĶéŗĶŅŅĻ©£¬Ń”ĻīA“ķĪó£»
B”¢ĖįŠŌKMnO4ČÜŅŗÄÜ°ŃŅŅĻ©Ńõ»ÆĪŖ¶žŃõ»ÆĢ¼£¬²»ÄܵƵ½“æ¾»ŅŅĶé£¬Ń”ĻīB“ķĪó£»
C”¢ŅŅĻ©ÓėäåĖ®·¢Éś¼Ó³É·“Ó¦£¬Éś³ÉŅŗĢ¬µÄ1,2-¶žäåŅŅĶ飬äåĖ®¼ČæÉŅŌÓĆĄ“¼ų±šŅŅĶéŗĶŅŅĻ©£¬ÓÖæÉŅŌÓĆĄ“³żČ„ŅŅĶéÖŠ»ģÓŠµÄŅŅĻ©£¬Ń”ĻīCÕżČ·£»
D”¢ŅŅĶéŗĶŅŅĻ©¶¼ÄÜČ¼ÉÕ£¬Ń”ĻīD“ķĪó”£
“š°øŃ”C”£


 ÖĒÄÜѵĮ·Į·²āæ¼ĻµĮŠ“š°ø
ÖĒÄÜѵĮ·Į·²āæ¼ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚÉ³Ä®ÖŠÅēČ÷Ņ»¶ØĮæµÄ¾Ū±ūĻ©Ėįõ„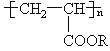 £¬”°Ė®ČÜŅŗ”±£¬ŹĒŅ»ÖÖŹ¹É³Ä®±äĀĢÖŽµÄŠĀ¼¼Źõ”£ĒėĶź³ÉĻĀĮŠÓŠ¹ŲĪŹĢā£ŗ
£¬”°Ė®ČÜŅŗ”±£¬ŹĒŅ»ÖÖŹ¹É³Ä®±äĀĢÖŽµÄŠĀ¼¼Źõ”£ĒėĶź³ÉĻĀĮŠÓŠ¹ŲĪŹĢā£ŗ
(1)ŗĻ³É¾Ū±ūĻ©Ėįõ„µÄµ„ĢåŹĒ_____________(Š“½į¹¹¼ņŹ½)”£
(2)øł¾Żõ„»Æ·“Ó¦µÄŌĄķ£¬Š“³öÖʱø¼×Ėį¼×õ„µÄ»Æѧ·“Ó¦·½³ĢŹ½_____________________”£
(3)±ūĻ©ŹĒŗĻ³É¾Ū±ūĻ©Ėįõ„µÄŌĮĻÖ®Ņ»£¬ĻĀĮŠĪļÖŹÄÜÓė±ūĻ©·“Ó¦µÄŹĒ___________”£
A.äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ B.ĒāŃõ»ÆÄĘČÜŅŗ
C.Cu(OH)2 Šü×ĒŅŗ D.ĖįŠŌøßĆĢĖį¼ŲČÜŅŗ
Š“³öĘäÖŠŅ»øö·“Ó¦µÄ»Æѧ·½³ĢŹ½_____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹Ųµ°°×ÖŹµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.ČĖ¹¤·½·Ø²»ÄÜŗĻ³É¾ßÓŠÉśĆü»īĮ¦µÄµ°°×ÖŹ
B.µ°°×ÖŹµÄ±äŠŌŹĒæÉÄę¹ż³Ģ
C.·ÖĄėµ°°×ÖŹŗĶĀČ»ÆÄʵĻģŗĻŅŗæɲÉÓĆ¹żĀĖµÄ·½·Ø
D.ÓĆĘ½ŠŠ¹āÕÕÉäµ°°×ÖŹČÜŅŗ£¬ŌŚ“¹Ö±ÓŚ¹āĻߵķ½ĻņæÉ擵½Ņ»Ģõ¹āĮĮµÄĶØĀ·
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗĻ½š¾ßÓŠŠķ¶ąÓÅĮ¼µÄĪļĄķ”¢»Æѧ»ņ»śŠµŠŌÄÜ”£ĻĀĮŠĪļÖŹŹōÓŚŗĻ½šµÄŹĒ
A. Ė®Ņų B. ²»ŠāøÖ C. ĢÕ“É D. ²£Į§
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹čŹĒĪŽ»ś·Ē½šŹō²ÄĮĻµÄÖ÷½Ē£¬¹čŌŖĖŲµÄµ„ÖŹ¼°Ęä»ÆŗĻĪļŌŚ»·¾³”¢ÄÜŌ“¼°²ÄĮĻæĘѧ֊ӊ×ÅÖŲŅŖÓ°ĻģŗĶ¹ć·ŗÓ¦ÓĆ”£ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)¹čŌŚ×ŌČ»½ēÖŠ×īÖ÷ŅŖµÄ“ęŌŚŠĪŹ½ŹĒ_______ŗĶ_______”£
(2)ÓŠĻĀĮŠĪļĢå»ņÉč±ø£ŗ¢ŁĖ®¾§¾µĘ¬ ¢Ś¼ĘĖ滜Š¾Ę¬ ¢ŪĀźč§ŹÖļķ ¢Ü¹čĢ«ŃōÄܵē³Ų ¢ŻŹÆÓ¢¹āµ¼ĻĖĪ¬”££ØÓĆŠņŗÅĢīŠ“£©ÓƵ½¹čµ„ÖŹµÄŹĒ_________£»ĖłÓĆ²ÄĮĻÖ÷ŅŖĪŖSiO2µÄŹĒ_________£»
(3)Š“³ö¹¤ŅµÉĻÖĘČ”“Ö¹čµÄ»Æѧ·“Ó¦·½³ĢŹ½___________”£ĘäÖŠ£¬Ńõ»Æ¼ĮĪŖ_____________£¬»¹Ō¼ĮĪŖ_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøßĢśĖįŃĪŌŚĖ®ČÜŅŗÖŠÓŠĖÄÖÖŗ¬ĢśŠĶĢ壬25”ꏱ£¬ĖüĆĒµÄĪļÖŹµÄĮæ·ÖŹżĖęPHµÄ±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹö“ķĪóµÄŹĒ
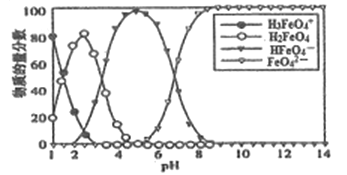
A. ŅŃÖŖH3FeO4+µÄµēĄėĘ½ŗā³£Źż·Ö±šĪŖ:K1=2.5”Į10-2£¬K2=4.8”Į10-4”¢K3=5.0”Į10-8.µ±pH=4Ź±£¬ČܶÉÖŠc(HFeO4-)/c(H2FeO4)=1.2
B. ĻņpH=5µÄøßĢśĖįŃĪČÜŅŗÖŠ¼ÓČėKOHČÜŅŗ£¬Ąė×Ó·½³ĢŹ½ĪŖHFeO4-+OH-=FeO42-+H2O
C. PH=2Ź±£¬ČÜŅŗÖŠÖ÷ŅŖŗ¬ĢśŠĶĢåÅØ¶ČµÄ“óŠ”¹ŲĻµĪŖc(H2FeO4)>c(H3FeO4+)>c(HFeO4-)
D. ĪŖ»ńµĆ¾”æÉÄÜ“æ¾»µÄøßĢśĖįŃĪ£¬Ó¦æŲÖĘPH”Ż9
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖĻĀĮŠČČ»Æѧ·½³ĢŹ½£ŗ2H2£Øg£©£«O2£Øg£©===2H2O£Øg£©£»¦¤H=£483£®6 kJ/mol
H2£Øg£©£«![]() O2£Øg£©===H2O£Øg£©£»¦¤H=£241£®8 kJ/mol
O2£Øg£©===H2O£Øg£©£»¦¤H=£241£®8 kJ/mol
H2£Øg£©£«![]() O2£Øg£©===H2O£Øl£©£»¦¤H=£285£®8 kJ/mol
O2£Øg£©===H2O£Øl£©£»¦¤H=£285£®8 kJ/mol
ŌņĒāĘųµÄČ¼ÉÕČČĪŖ
A. 438£®6 kJ/mol B. 241£®8 kJ/mol C. 285£®8 kJ/mol D. ĪŽ·ØČ·¶Ø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijKClѳʷ֊ŗ¬ÓŠÉŁĮæK2CO3”¢K2SO4ŗĶ²»ČÜÓŚĖ®µÄŌÓÖŹ”£ĪŖĮĖĢį“æKCl£¬ĻČ½«ŃłĘ·ČÜÓŚŹŹĮæĖ®ÖŠ£¬½Į°č”¢¹żĀĖ£¬ŌŁ½«ĀĖŅŗ°“ĻĀĶ¼ĖłŹ¾²½Öč½ųŠŠĢį“æ(¹żĀĖ²Ł×÷ŅŃĀŌČ„)”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A£®ĘšŹ¼ĀĖŅŗ³£ĪĀĻĀpH£½7 B£®ŹŌ¼Į¢ńĪŖBa(NO3)2ČÜŅŗ
C£®ÉĻĶ¼¹ż³ĢŠė¾2“Ī¹żĀĖ D£®²½Öč¢ŪÄæµÄŹĒ³żČ„CO32£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”¢B”¢C”¢D”¢EĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£»AŌŖĖŲµÄŌ×Ó°ė¾¶×īŠ”£»BŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļÓėĘäĒā»ÆĪļÄÜÉś³ÉŃĪ£»DÓėAĶ¬Ö÷×壬ĒŅÓėEĶ¬ÖÜĘŚ£»EŌŖĖŲŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒĘä“ĪĶā²ćµē×ÓŹżµÄ3/4£»A”¢B”¢D”¢EÕāĖÄÖÖŌŖĖŲ£¬ĆæŅ»ÖÖÓėCŌŖĖŲ¶¼ÄÜŠĪ³ÉŌ×ÓøöŹż±Č²»ĻąĶ¬µÄČōøÉÖÖ»ÆŗĻĪļ”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©BŗĶAŠĪ³ÉµÄ10µē×Ó»ÆŗĻĪļµÄµē×ÓŹ½ŹĒ_______
£Ø2£©A”¢B”¢C”¢EæÉŠĪ³ÉĮ½ÖÖĖįŹ½ŃĪ£Ø¾łÓÉĖÄÖÖŌŖĖŲ×é³É£©£¬Į½ÖÖĖįŹ½ŃĪĻą»„·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_________
£Ø3£©A”¢C”¢E¼äæÉŠĪ³É¼×”¢ŅŅĮ½ÖÖĪ¢Į££¬ĖüĆĒ¾łĪŖøŗŅ»¼ŪĖ«Ō×ÓŅõĄė×Ó£¬ĒŅ¼×ÓŠ18øöµē×Ó£¬ŅŅÓŠ10øöµē×Ó£¬Ōņ¼×ŗĶŅŅ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ________
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com