
有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为:
A.A>B>C>D B.C>A>B>D C.A>C>D>B D.B>D>C>A
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使得甲醚在制药、燃料、农药等化学工业中有许多独特的用途。
(1)已知:2CH3OH(g)CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol·L-1) | 0.8 | 1.24 | ? |
①平衡时,c(CH3OCH3)等于________ mol·L-1,反应混合物的总能量减少________ kJ。
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的转化率和浓度的曲线示意图。

(2)在直接以甲醚为燃料的电池中,电解质溶液为酸性,负极的反应为________________、正极的反应为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车为期中含有氮的氧化物,它是城市空气的污染源之一.汽车行驶时,由于点火化的作用,在汽缸里发生了一系列的化学反应,其中有N2+O2 2NO;2NO+O2=2NO2;这两个反应都属于()
2NO;2NO+O2=2NO2;这两个反应都属于()
| A. | 分解反应 | B. | 置换反应 | C. | 化合反应 | D. | 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知MnO2与浓盐酸可以发生如下反应:
4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O,若产生7.1gCl2,则:
MnCl2+Cl2↑+2H2O,若产生7.1gCl2,则:
(1)参加反应的HCl是多少克?
(2)被氧化的HCl是多少克?
(3)参加反应的MnO2物质的量是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个小烧杯里,加入约20 g已研磨成粉末的氢氧化钡晶体,将小烧杯放在事先已滴有3—4滴水的玻璃片上,然后再加入约10 g NH4Cl晶体,并立即用玻璃棒迅速搅拌。试完成下列问题:
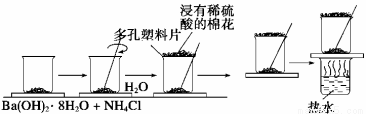
(1)写出有关反应方程式 ,该反应属于 反应。(填基本反应类型)
(2)实验中要立即用玻璃棒迅速搅拌的原因是__ 。
(3)如果实验中没有看到“结冰”现象,可能的原因是(列举三条) 。
(4)“结冰”现象说明了该反应是 热(填“放”或“吸”),反应物的总能量比生成物的总能量 (填“高”或“低”);
(5)在上述实验过程中,用浸有稀硫酸的湿棉花置于多孔塑料板上的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)_______>__________;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______>__________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________。
(4)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:___________________。
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
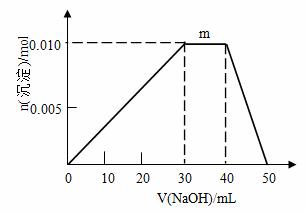
①R离子浓度由大到小的顺序是:__________。
②写出m点反应的离子方程式_________________。
③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
硒(Se)是人体必需的微量元素,在元素周期表中的位置如下图。下列关于硒元素的叙述正确的是
A. 硒位于元素周期表第四周期第IVA族
B. 硒的非金属性比S弱
C. H2Se比HBr稳定
D. 最高价氧化物的化学式为SeO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com