
分析 4HCl(浓)+MnO2 $\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O中,Mn元素的化合价由+4价降低为+2价,HCl中Cl元素的化合价由-1价升高为0,以此来解答.
解答 解:4HCl(浓)+MnO2 $\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O中,Mn元素的化合价从+4价降为+2价得电子被还原,则MnO2为氧化剂,HCl中Cl元素的化合价-1价升高为0价,失去电子被氧化,则HCl为还原剂,所以生成氧化产物为Cl2,氧化剂与还原剂的物质的量之比是1:2,可通过双线桥分析此氧化还原反应, ;
;
故答案为:(1)Cl;Mn;(2)MnO2;Cl2;(3)1:2;(4) .
.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,注意元素的化合价判断及守恒法应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用25mL量筒量取12.36mL盐酸 | |
| B. | 用托盘天平称量8.75g食盐 | |
| C. | 测得某温度下硝酸钾的溶解度是36.5g | |
| D. | 用广泛pH试纸测得某溶液的pH为3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高压钠灯常用于道路和广场的照明 | |
| B. | 钠钾合金可在快中子反应堆中作热交换剂 | |
| C. | 工业上通过电解氯化钠溶液制取金属钠 | |
| D. | 钠可用于从钛、铌等金属的氯化物中置换出金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有的盐电离时只能生成酸根阴离子和金属阳离子 | |
| B. | 只由一种分子组成的物质一定为纯净物,组成混合物的物质可能只有一种元素 | |
| C. | 氧化物是指含有氧元素的化合物,如NaOH、H2SO4等 | |
| D. | 氨气溶于水溶液显碱性,所以氨气属于碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

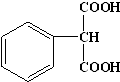 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com