
| A. | 增大压强,单位体积活化分子数一定增加,化学反应速率一定增大 | |
| B. | 升高温度,活化分子百分数增加,化学反应速率一定增大 | |
| C. | 加入反应物,使活化分子百分数增加,化学反应速率增大 | |
| D. | 使用催化剂,一定降低了反应的活化能,化学反应速率一定增大 |
分析 A.增大压强,单位体积内活化分子个数不一定增加,化学反应速率不一定增大;
B.升高温度,增大活化分子百分数,反应速率增大;
C.加入反应物,活化分子百分数不增加,反应速率不一定增大;
D.使用催化剂,改变反应所需活化能,化学反应速率改变.
解答 解:A.增大压强,单位体积内活化分子个数不一定增加,化学反应速率不一定增大,如恒容条件下加入稀有气体,体系压强增大但反应物和生成物浓度不变,活化分子个数不变,反应速率不变,故A错误;
B.升高温度,使部分非活化分子转化为活化分子,增大活化分子百分数,反应速率增大,故B正确;
C.加入反应物,活化分子百分数不变,反应速率不一定增大,如果反应物是固体,反应物量的多少不影响反应速率,故C错误;
D.使用催化剂,改变反应所需活化能,化学反应速率改变,如果该催化剂是负催化剂,则能降低反应速率,故D错误;
故选B.
点评 本题考查化学反应速率影响因素,为高频考点,明确外界条件对化学反应速率影响原理及其适用条件是解本题关键,易错选项是BD,注意特殊情况,题目难度不大.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:选择题
| A. | 纯净的氧气 | B. | 过氧化氢 | C. | 过氧化钠 | D. | 过氧化钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,在周期表中的位置第四周期ⅢB族,属于d区.
,在周期表中的位置第四周期ⅢB族,属于d区.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5mol | B. | 4mol | C. | 6mol | D. | 3.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C5H12的同分异构体中,其中的一种只能生成一种一氯代物 | |
| B. | CH3-CH﹦CH-C≡C-CF3分子结构中6个碳原子不可能都在同一平面上 | |
| C. | 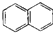 不属于脂环化合物 不属于脂环化合物 | |
| D. | 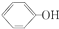 和 和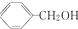 不是同系物 不是同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com