
【题目】Ⅰ.火箭升空需要高能的燃料,经常是用N2O4和N2H4作为燃料,工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等。已知:
N2(g) + 2O2(g)=2NO2(g) △H= +67.7kJ·mol-1
N2H4(g) + O2(g)=N2(g) + 2H2O(g) △H=-534.0kJ·mol-1
NO2(g)![]() 1/2N2O4(g) △H=-26.35kJ·mol-1
1/2N2O4(g) △H=-26.35kJ·mol-1
试写出气态联氨在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:___。
Ⅱ.1100℃时,体积为2L的恒容容器中发生如下反应:Na2SO4(s)+4H2(g)![]() Na2S(s)+4H2O(g)。
Na2S(s)+4H2O(g)。
(1)下列能判断反应达到平衡状态的是____。
A.容器中压强不变 B.混合气体密度不变
C.1molH-H键断裂同时形成2 mol H-O D.H2的体积分数不变
(2)若2min时反应达平衡,此时气体质量增加8g,则用H2表示该反应的反应速率为___。
(3)某温度下该反应达平衡状态,测得混合气体的平均相对分子质量为14,则该温度下的平衡常数K为_____。
(4)若反应达平衡后,加入少量的H2,再次平衡后,H2O的体积分数___(填“增大”、“减小”或“不变”)。
【答案】2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H=-1083.0kJ·mol-1 BD 0.125mol/(L·min) 81 不变
【解析】
Ⅰ.依据盖斯定律计算可得;
Ⅱ.(1)可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化;
(2)根据气体增加的质量与氢气之间的关系计算氢气的平均反应速率;
(3)依据平均相对分子质量计算平衡时氢气和水蒸气的物质的量比,再依据化学平衡常数公式计算;
(4)若反应达平衡后,加入少量的氢气,平衡向正反应方向移动,因温度不变化学平衡常数不变,所以再次平衡后,氢气和水的物质的量比不变。
Ⅰ.将已知反应依次编号为①②③,根据盖斯定律可知,②×2-①-③×2得2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g),故△H=2×(-534.0kJmol-1)-67.7kJmol-1-2×(-26.35kJmol-1)=-1083.2kJmol-1,故答案为:2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1083.0 kJ/mol;
Ⅱ.(1)A、该反应是一个气体体积不变的反应,无论反应是否达到平衡状态,容器中压强始终不变,容器中压强不变不能据此判断是否达到平衡状态,故错误;
B、该反应是一个气体质量增大的反应,当恒容容器中混合气体密度不变时,说明反应达到平衡状态,故正确;
C、无论反应是否达到平衡状态,都存在1mol H-H键断裂同时形成2mol H-O,1molH-H键断裂同时形成2 mol H-O不能据此判断是否达到平衡状态,故错误;
D、H2的体积分数不变时,说明正逆反应速率相等,反应达到平衡状态,故正确;
BD正确,故答案为:BD;
(2)第2min时,气体质量增加8g,由方程式可知参加反应的氢气的物质的量为![]() mol=0.5mol,则氢气的平均反应速率
mol=0.5mol,则氢气的平均反应速率![]() =0.125mol/(L.min),故答案为:0.125mol/(L·min);
=0.125mol/(L.min),故答案为:0.125mol/(L·min);
(3)某温度下该反应达平衡状态,测得混合气体的平均相对分子质量为14,设氢气的物质的量为xmol、水蒸气的物质的量为ymol,则平均相对分子质量=![]() =14,解得x:y=1:3,即同一容器中氢气和水的浓度之比为1:3,则该温度下的平衡常数K=
=14,解得x:y=1:3,即同一容器中氢气和水的浓度之比为1:3,则该温度下的平衡常数K=![]() =
=![]() =81,故答案为:81;
=81,故答案为:81;
(4)若反应达平衡后,加入少量的氢气,平衡向正反应方向移动,因温度不变化学平衡常数不变,所以再次平衡后,氢气和水的物质的量比不变,则水的体积分数不变,故答案为:不变。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
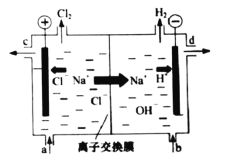
完成下列填空:
(1)写出电解饱和食盐水的离子方程式_______。
(2)离子交换膜的作用为:______、______。
(3)精制饱和食盐水从图中_____位置补充,氢氧化钠溶液从图中_____位置流出(选填“a”、“b”、“c”或“d”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制95mL 1 mol·L-1的稀硫酸。

可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。
请回答下列问题:
(1)盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的_______。

(2)配制稀硫酸时,除玻璃棒外还缺少的仪器是________________(写仪器名称);
(3)经计算,配制95mL1 mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为______mL,量取硫酸时应选用_________mL规格的量筒(填序号);
A.10 mL B.50 mL C.100 mL D.200mL
(4)取25 mL1 mol·L-1的硫酸,向其中加入一定量的氧化铜,充分反应后制得硫酸铜溶液。用该溶液制取CuSO4·5H2O,所需要的主要玻璃仪器除酒精灯、玻璃棒外,还缺少的仪器是___________;
(5)对所配制的稀硫酸进行测定,发现其浓度大于1 mol·L-1,配制过程中下列各项操作可能引起该误差的原因__________(填序号)。
A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
C.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作
D.转移溶液时,不慎有少量溶液洒到容量瓶外面
E.定容时,俯视容量瓶刻度线进行定容
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示的反应判断下列说法中错误的是

A. CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量
B. 该反应的焓变大于零
C. 该反应中有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键生成放出能量
D. 由该反应可推出凡是需要加热才发生的反应均为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着钴酸锂电池的普及使用,从废旧的钴酸锂电池中提取锂、钴等金属材料意义重大。如图是废旧钻酸锂(LiCoO2)(含少量铁、铝、铜等元素的化合物)回收工艺流程:
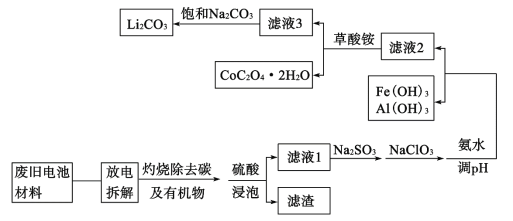
(1)“拆解”前需进入“放电”处理的目的是__;用食盐水浸泡是放电的常用方法,浸泡放电过程中产生的气体主要有__。
(2)上述流程中将CoO2-转化为Co3+的离子方程式为__。
(3)滤液1中加入Na2SO3的主要目的是__;加入NaClO3的主要目的是__。
(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如图所示:

根据图沉钴时应控制n(C2O42-):n(Co2+)比为__,温度控制在__℃左右。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑
B.AlCl3溶液中加入过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
C.三氯化铁溶液中加入金属钠:3Na+Fe3+=3Na++Fe
D.NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量Fe、FeO、Fe2O3的混合物中,加入50mL1mol·L-1硫酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的混合物,能得到铁的质量为
A. 11.2g B. 2.8g C. 5.62g D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有碳酸钠、碳酸氢钠的混合物19.0g,把它们加热到质量不再减轻,冷却后称量为15.9g。求:
(1)原混合物中碳酸钠的质量分数_________。(写出计算过程,结果保留3位有效数字)
(2)将原混合物19.0g完全溶解于蒸馏水水中,配成500mL溶液,则其中钠离子物质的量浓度为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗盐中常含 Ca2+、Mg2+、SO42-以及泥沙等杂质,一种制备精盐的实验方案及步骤如下(用于沉淀的试剂饱和 Na2CO3 溶液、BaCl2 溶液、NaOH 溶液均稍过量):
![]()
(1)若试剂①选用 NaOH 溶液,则试剂②产生的沉淀的化学式为 ___________。判断滴加试剂③ 已过量的方法是:__________。
(2)操作Ⅱ为___________。溶液丙中,溶质除 NaCl 外还含有____________(填化学式)等。
(3)食用盐常在精盐中加入 KIO3。为了检验实验中是否含 KIO3,可以用以下反应进行:KIO3+5KI+3H2SO4![]() 3I2+3K2SO4+3H2O。
3I2+3K2SO4+3H2O。
①用双线桥分析以上反应中电子转移的方向和数目:_____。
②反应中氧化剂与还原剂的物质的量之比为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com