
����Ŀ���ϳɹ�̽���һ��·�����£�
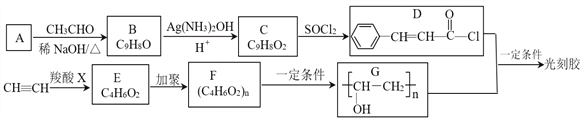
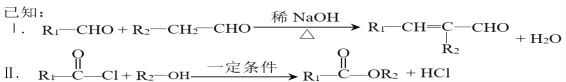
��RCOOH+CH![]() CH��RCOOCH=CH2
CH��RCOOCH=CH2
�ش���������
��1����̽������������ŵ�������______��
��2��D+G����̽��Ļ�ѧ����ʽΪ______���÷�Ӧ�ķ�Ӧ������______��
��3��H��C��ͬ���칹�壬H�����������ʻ����������ܷ���ˮ�ⷴӦ��������Ӧ������ʹ��ˮ��ɫ�������ڷ����廯�����H�Ľṹ��______�֡����к˴Ź�������Ϊ5��壬�ҷ������Ϊ1��1��2��2��2�Ľṹ��ʽΪ______��
��4����������֪ʶ����������Ϣ��д����CH3CH2OHΪԭ���Ʊ�CH3CH2CH2COOC2H5�ĺϳ�·������ͼ(���Լ���ѡ)��
���ϳ�·������ͼʾ�����£�![]() ��
��
______
���𰸡� ̼̼˫�������� 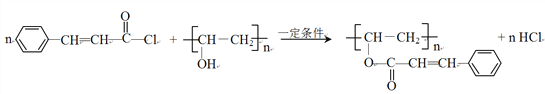 ȡ����Ӧ 5
ȡ����Ӧ 5 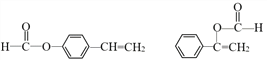 CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH![]() CH3CH2CH2COOH
CH3CH2CH2COOH![]() CH3CH2CH2COOC2H5
CH3CH2CH2COOC2H5
�����������ݸ����ʵ�ת����ϵ��A������Ϣ���еķ�Ӧ����B��B����������Ӧ����C��C����ȡ����Ӧ����D������D�Ľṹ��ʽ��֪��CΪ![]() ��BΪ
��BΪ![]() ��AΪ
��AΪ![]() ��������Ϣ�����E�ķ���ʽ��֪������XΪCH3COOH��EΪCH3COOCH=CH2��E�����Ӿ۷�Ӧ����FΪ
��������Ϣ�����E�ķ���ʽ��֪������XΪCH3COOH��EΪCH3COOCH=CH2��E�����Ӿ۷�Ӧ����FΪ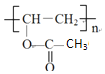 ��F����ȡ������G��G��D����ȡ����Ӧ���ɹ�̽�Ϊ
��F����ȡ������G��G��D����ȡ����Ӧ���ɹ�̽�Ϊ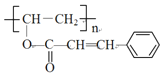 ��
��
��1����̽�Ϊ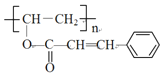 �������������ŵ�������̼̼˫�����������ʴ�Ϊ��̼̼˫����������
�������������ŵ�������̼̼˫�����������ʴ�Ϊ��̼̼˫����������
��2����������ķ�����֪��G��D����ȡ����Ӧ���ɹ�̽�Ϊ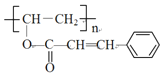 ����Ӧ�Ļ�ѧ����ʽΪ
����Ӧ�Ļ�ѧ����ʽΪ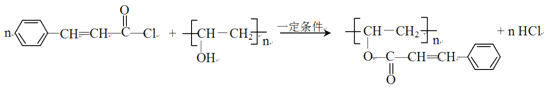 ���ʴ�Ϊ��
���ʴ�Ϊ��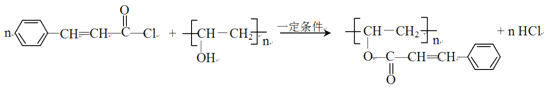 ��ȡ����Ӧ��
��ȡ����Ӧ��
��3��CΪ![]() ��H��C��ͬ���칹�壬T�����������ʻ����������ܷ���ˮ�ⷴӦ��������Ӧ��˵���м���ij��������ʹ��ˮ��ɫ��˵����̼̼˫���������ڷ����廯���˵���б���������������ĽṹΪ����������HCOOCH=CH-����HCOOC��=CH2��-������������������ΪHCOO-��-CH=CH2����3�ֽṹ�����Թ���5�֣����к˴Ź�������Ϊ5��壬�ҷ������Ϊ1��1��2��2��2�Ľṹ��ʽΪ
��H��C��ͬ���칹�壬T�����������ʻ����������ܷ���ˮ�ⷴӦ��������Ӧ��˵���м���ij��������ʹ��ˮ��ɫ��˵����̼̼˫���������ڷ����廯���˵���б���������������ĽṹΪ����������HCOOCH=CH-����HCOOC��=CH2��-������������������ΪHCOO-��-CH=CH2����3�ֽṹ�����Թ���5�֣����к˴Ź�������Ϊ5��壬�ҷ������Ϊ1��1��2��2��2�Ľṹ��ʽΪ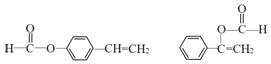 ���ʴ�Ϊ��5��
���ʴ�Ϊ��5��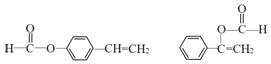 ��
��
��4����CH3CH2OHΪԭ���Ʊ�CH3CH2CH2COOH����CH3CH2OH������CH3CHO��CH3CHO��ϡ�������Ƶ�����������CH3CH=CHCHO���������ӳɵ�CH3CH2CH2CH2OH���ٽ�CH3CH2CH2CH2OH������CH3CH2CH2COOH����������Ҵ��������ɣ��ϳ�·��ΪCH3CH2OH ![]() CH3CHO
CH3CHO![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH ![]() CH3CH2CH2COOH
CH3CH2CH2COOH![]() CH3CH2CH2COOC2H5���ʴ�Ϊ��CH3CH2OH
CH3CH2CH2COOC2H5���ʴ�Ϊ��CH3CH2OH ![]() CH3CHO
CH3CHO![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH![]() CH3CH2CH2COOH
CH3CH2CH2COOH![]() CH3CH2CH2COOC2H5��
CH3CH2CH2COOC2H5��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й����ʵ�ת����ϵ����ͼ��ʾ������������ͷ�Ӧ��������ȥ����D��F��G��H��Ϊ�������壬����D��ʹʪ��ĺ�ɫʯ����ֽ������G�ʻ���ɫ��H�ڿ����к�����ߣ�C��Ħ������Ϊ32g��mol-1��EΪ�����Լ

��1��C�Ļ�ѧʽΪ_______________��
��2��H�ĵ���ʽΪ____________________��
��3��д����Ӧ�ٵ����ӷ���ʽ��___________________��
��4��д����Ӧ�ڵĻ�ѧ����ʽ��____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���Ԫ�����ʻ�ԭ�ӽṹ�ݱ������ȷ����(����)
A. Li��Be��Bԭ��������������������
B. N��O��FԪ����������ϼ���������
C. P��S��Clԭ�Ӱ뾶��������
D. Na��K��Rb�ĵ��Ӳ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��0.01molL��1��ijһԪ������Һ pH=4�������ĵ����Ϊ�� ��
A.1%
B.2%
C.5%
D.10%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������ƶ��������ӵ���
A. �Ȼ��ƾ��� B. �ۻ����Ȼ��� C. �������Һ D. Һ̬�Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȩΪԭ�Ͽɺϳɸ߷���Ϳ��PMA��PVAC���ϳ�·�����£�

��1��������A�����������ŵ�������___________��___________��
��2��������C��E�Ĺ�ϵ��___________��
��3���ܵķ�Ӧ������___________���ķ�Ӧ������___________��
��4��PVAC�Ľṹ��ʽΪ___________��
��5����Ӧ�۵Ļ�ѧ����ʽΪ___________����Ӧ�ݵĻ�ѧ����ʽΪ��ע����Ӧ������___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Һ�������ͺ��Ȼ�����Һ�����Ҵ������Ȼ�̼��Һ�Ļ������Ȼ��ƺ͵��ʵ��ˮ��Һ���������ϻ�������ȷ���������ǣ� ��
A. ��Һ����ȡ������ B. ��ȡ������Һ
C. ��Һ��������ȡ D. ������ȡ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������ij�л�����������Ʒ�Ӧ���ɵõ�����VA L���������ĸ��л����������Ĵ�����Һ��Ӧ���ɵõ�����VB L����ͬ�¡�ͬѹ��VA��VB �� ����л�������ǣ� ��
A.HO��CH2��2CHO
B.HO��CH2��2COOH
C.HOOC��COOH
D.CH3COOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�ӦNO2(g)+SO2(g)![]() SO3(g)+NO(g)+Q��Q��0���ɴ���NO2��SO2�ȴ�����Ⱦ�����ʮ����Ҫ�����塣
SO3(g)+NO(g)+Q��Q��0���ɴ���NO2��SO2�ȴ�����Ⱦ�����ʮ����Ҫ�����塣
���������գ�
��1���÷�Ӧ�б�������Ԫ����__________��д���÷�Ӧ��ƽ�ⳣ������ʽ��K =_____________��
��2����������Ӧ��һ�ܱ������н��С������ܱ�����Ӧ�ﵽƽ��״̬����_______��ѡ��������
a�����������ɫ���ֲ���
b��NO2��NO������ȱ��ֲ���
c��ÿ����1mol SO2��ͬʱ����1mol SO3
d����ϵ�������ܶȱ��ֲ���
��3��һ���¶��£����ݻ�ΪV L������������������Ӧ��t min�ڣ�SO2�����ʵ����½���a mol�������ʱ����v(NO) =__________���������ĸ��ʾ��ע����λ����
��4����д�����������SO2ת���ʵĴ�ʩ��_____________��_____________��
��5����������Һ���ã�pH���С�����÷���ʽ��ʾ��ԭ��_______________
��6����SO2����ͨ��NaOH��Һ������Һ��SO32����Ũ�ȱ仯��ͼ��ʾ�������ԭ��
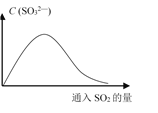
__________________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com