
(8分)请根据反应:Fe + Cu2+ = Fe 2++ Cu 设计原电池:
(1) (2分)画出实验的简易装置图:(用铅笔画图)
(2)(6分)写出电极反应式,正极: ,负极: 。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是 。
科目:高中化学 来源: 题型:阅读理解

 请根据以上流程,回答相关问题:
请根据以上流程,回答相关问题:| 化学式 | BaCO3 | BaSO4 | Ca SO4 | MgCO3 | Mg(OH)2 |
| Ksp | 8.1×10一9 | 1.08×10一10 | 1.9×10一4 | 3.5×10一5 | 1.6×10一11 |

查看答案和解析>>
科目:高中化学 来源: 题型:
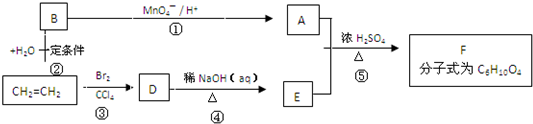
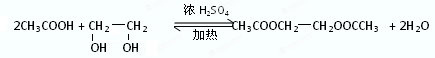

| 醇 |
| △ |
| 醇 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)请根据反应 :Fe + Cu2+ = Fe 2++Cu 设计原电池:
(1) (2分)画出实验的简易装置图:(用铅笔画图)
(2)(6分)写出电极反应式,正极: ,负极: 。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是 。
查看答案和解析>>
科目:高中化学 来源:2014届广东省高一下学期期中考试化学试卷(解析版) 题型:填空题
(8分)请根据反应 :Fe + Cu2+ = Fe 2++ Cu 设计原电池:
(1) (2分)画出实验的简易装置图:(用铅笔画图)
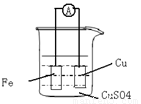
(2)(6分)写出电极反应式,正极: ,负极: 。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com