
| A、2.5mol |
| B、1mol |
| C、0.5mol |
| D、0.25mol |


科目:高中化学 来源: 题型:
| A、胶体是带电的,溶液是电中性的 |
| B、向煮沸的1mol/LNaOH溶液 中滴加FeCl3饱和溶液得Fe(OH)3胶体 |
| C、依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
| D、向污水投放明矾,能生成凝聚悬浮物的胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
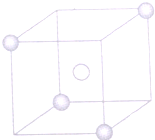 某离子晶体的晶胞结构如图所示,X(●)位于立方体的顶点,Y(○)位于立方体的中心,试分析:
某离子晶体的晶胞结构如图所示,X(●)位于立方体的顶点,Y(○)位于立方体的中心,试分析:查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验内容 | 实验目的 |
| A | 在滴有酚酞的Na2CO3溶液中, 加入BaCl2溶液后红色褪去 | 验证Na2CO3溶液中存在水解平衡 |
| B | 在未知溶液中加入稀盐酸和氯化钡溶液有沉淀生成 | 说明该未知溶液含有SO42- |
| C | 用玻璃棒蘸取氯水点在pH是指中央 | 检验氯水呈酸性 |
| D | 将C与浓硫酸反应后的气体直接通入石灰水 | 证明反应有CO2生成 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
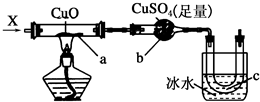 按照如图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体或蒸气可能是(假设每个反应均完全)( )
按照如图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体或蒸气可能是(假设每个反应均完全)( )| A、CH3CH2OH |
| B、CO或H2 |
| C、NH3 |
| D、C(CH3)3(OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能使润湿的碘化钾淀粉试纸变蓝的气体一定是Cl2 |
| B、能使澄清石灰水变浑浊的无色气体一定是CO2 |
| C、在潮湿空气中能形成白雾的气态氢化物一定是HCl |
| D、溶于水能形成无色溶液的红棕色气体一定是NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、La和盐酸反应的离子方程式为:La+2H+=La3++H2↑ |
| B、LaCl3的水溶液加热蒸发灼烧,最终得到无水LaCl3 |
| C、镧有两种核素:57139La和放射性57138La,由此可知镧元素的相对原子质量为138.5 |
| D、La(NO3)3水溶液显酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com