
ҽ�����̷�(FeSO4•7H2O)������ȱ����ƶѪ����Чҩ��ij��ѧ��ȤС����̷����������µ�̽����
���Ʊ���Ʒ��
��С���ɷ���м(����������ͭ��������������)������ͼ��ʾװ���Ʊ� FeSO4 •7H2O���壬�������£�
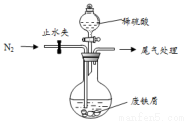
��1��Ԥ�������Ƚ�����м���뵽���� Na2CO3��Һ��ϴ�ӣ�Ŀ����__________ ��Ȼ����м��ˮϴ�� 2��3 �顣
��2����ϴ�Ӻ�ķ���м���뵽Բ����ƿ�У�������ͨ��N2
��3���ټ�������ϡ���ᣬ�����¶� 50�桫80��֮�䣬��ַ�Ӧ��Բ����ƿ��ʣ��Ĺ���Ϊ__________ ��ʵ���ҳ������軯����Һ���鷴Ӧ���ɵ�Fe2+��д���÷�Ӧ�����ӷ�Ӧ����ʽ��______________��
��4����ȡ��Ʒ�������裨3���з�Ӧ��Ļ�����м�����������ˮ�����ȹ��ˣ���ȴ�ᾧ���˳����壬��������ˮϴ�� 2��3 �Σ�������ֽ���������ɣ��ܱձ��档
���ⶨFeSO4 •7H2O ������
��1����ȡ������Ʒ 10.0g������������ϡ�����У���� 100mL ��Һ��ȷ��ȡ 25.00mL ��Һ������ƿ�У��� 0.1000mol/L KMnO4����Һ�ζ��ζ�3�Σ�ƽ������ 10.00mL��Һ������Ʒ�� FeSO4 •7H2O ����������Ϊ________ ��(��֪ Mr(FeSO4 •7H2O)=278)��
��2�����������ƫС����������ڶ���ʱ________(����ӡ������ӡ�)������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�����������и���4���ʼ����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
NAΪ�����ӵ�������ֵ������˵���У���ȷ����
A�����³�ѹ�£�l.6g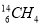 �к��й��ۼ�����Ϊ0.4NA
�к��й��ۼ�����Ϊ0.4NA
B���ܱ�������2molNO��1molO2��ַ�Ӧ������������ķ�����Ϊ2NA
C��1L0.lmol��L-1��CH3COONa��Һ��CH3COO-��CH3COOH������֮��Ϊ0.1NA
D������������ˮ��Ӧʱ������0.1mol����ת�Ƶĵ�����Ϊ0.4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�ڿ�ǰ��ϰ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��ij�¶��£���������ʼ�����Ϊ1L���ܱ������а��±���ʾͶ�ϣ�������Ӧ��2SO2(g)+O2(g) 2SO3(g) ��H��0���ﵽƽ���������˵����ȷ����
2SO3(g) ��H��0���ﵽƽ���������˵����ȷ����
������� | �������� | ��ʼ���ʵ���/mol | ƽ��ʱSO3�����ʵ���/mol | ||
SO2 | O2 | SO3 | |||
�� | ���º��� | 2 | 1 | 0 | 1.2 |
�� | ���Ⱥ��� | 0 | 0 | 2 | a |
�� | ���º�ѹ | 2 | 1 | 0 | b |
A��ƽ��ʱSO3�����ʵ�����a��1.2��b��1.2
B����������ƽ�ⳣ����ͬ
C������ I��SO2��ת��������������SO3��ת����֮��С��1
D������ʼʱ���������г���1.0mol SO2 (g)��0.40mol O2(g)��1.40mol SO3 (g)�����ʱ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������������и�����ģ���ۻ�ѧ�Ծ��������棩 ���ͣ������
����ѧ-ѡ��2����ѧ�뼼����
�Ȼ���ͭ(CuCl)�㷺Ӧ���ڻ�����ӡȾ����Ƶ���ҵ��CuCl�����ڴ���ˮ��������������Ũ�Ƚϴ����ϵ���ڳ�ʪ��������ˮ���������Ժ���ͭ(��Ҫ�ɷ���Cu������CuO)Ϊԭ�ϲ�������������ֽ⼼������CuC1�Ĺ��չ������£�
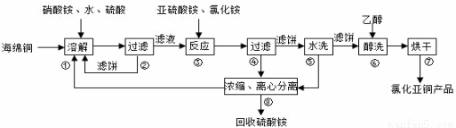
�ش��������⣺
��1��������еõ�������������___________���ܽ��¶�Ӧ������60-70�棬ԭ����___________��
��2��д�����������Ҫ��Ӧ�����ӷ���ʽ_________________��
��3������ݰ�����pH=2����ϴ��ˮϴ������������ϴ���õ�����__________(д����)��
��4�����������У��������ʡ�ԣ�������_________________��
��5������ڡ��ܡ��ݡ��Ҫ���й�Һ���룮��ҵ�ϳ��õĹ�Һ�����豸��_______(����ĸ)
A�������� B�����Ļ� C����Ӧ�� D����ʽѹ�˻�
��6��ȷ��ȡ���Ʊ����Ȼ���ͭ��Ʒmg���������ڹ�����FeCl3��Һ�У�����Ʒ��ȫ�ܽ��������ϡ���ᣬ��amol/L-1��K2Cr2O7��Һ�ζ����յ㣬����K2Cr2O7��ҺbmL����Ӧ��Cr2O72-����ԭΪCr3+����Ʒ��CuCl����������Ϊ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������������и�����ģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʽΪC4H8O2����������������Һ��Ӧ���л���(�����������칹��ȩ������)��
A��2�� B��4�� C��6�� D��8��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ��ɶ�ʯ����ѧ�߶�4���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��t��ʱAgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ��t��ʱAgCl��Ksp��4��10��10������˵������ȷ����
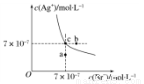
A����t��ʱ��AgBr �� KspΪ4.9��10��13
B���� t ��ʱ��AgCl(s)��Br��(aq) AgBr(s)��Cl��(aq)��ƽ�ⳣ�� K��816
AgBr(s)��Cl��(aq)��ƽ�ⳣ�� K��816
C��ͼ��a���Ӧ����AgBr�IJ�������Һ
D���� AgBr ������Һ�м���NaBr���壬��ʹ��Һ��c��䵽b��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ��ɶ�ʯ����ѧ�߶�4���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������ڽ����ơ�������Ͷ�����(Na2Sx)�ֱ���Ϊ�����缫�ķ�Ӧ�����Al2O3�մ�(�ɴ���Na��)Ϊ����ʣ��䷴Ӧԭ����ͼ��ʾ������˵����ȷ����
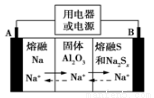
A����������A�缫���õ�����B�缫������ʡ�A �缫
B�����ʱ���缫B����ӵ�Դ�����������缫��ӦʽΪ Sx2-��2e��=xS
C�����øõ���������϶�п��������Ӧ��B�缫������
D�����øõ�ص�⾫��ͭ����·��ת��1mol����ʱ��������������32 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʯ��ɽ���и�������ģ���ۻ�ѧ�Ծ��������棩 ���ͣ������
���������������Ƚ������ⷽ������������������������������Ӧϵͳͬʱͨ����顢������ˮ��������������Ҫ��ѧ��Ӧ�У�
��Ӧ ���� | ��ѧ����ʽ | �ʱ��H ��kJ/mol�� | ����Ӧ���Ea ��kJ/mol�� |
���� ����[ | CH4��g����2O2��g����CO2��g����2H2O��g�� | ��802��6 | 125��6 |
CH4��g����O2��g����CO2��g����2H2��g�� | ��322��0 | 172��5 | |
���� ���� | CH4��g����H2O��g����CO��g����3H2��g�� | 206��2 | 240��1 |
CH4��g����2H2O��g����CO2��g����4H2��g�� | 165��0 | 243��9 |
�ش��������⣺
��1����ӦCO��g����H2O��g����CO2��g����H2��g���ġ�H= kJ/mol��
��2���ڳ�ʼ��,�������������ķ�Ӧ���� ���������ķ�Ӧ���ʣ�����ڡ�С�ڻ���ڣ���
��3���������෴Ӧ����ij��֣�B����ƽ��ѹǿ��PB���������ʵ���Ũ�ȣ�cB��Ҳ�ɱ�ʾƽ�ⳣ��������KP������ӦCH4��g����H2O��g�� CO��g����3H2��g��KP�ı���ʽΪ �������¶ȵ����ߣ���ƽ�ⳣ�� �����������С�����䡱����
CO��g����3H2��g��KP�ı���ʽΪ �������¶ȵ����ߣ���ƽ�ⳣ�� �����������С�����䡱����
��4���������Ƕȷ������������������������Ƚ�֮������ ��
��5����ijһ�������ϱȵ�����£��¶ȡ�ѹǿ��H2��CO���ʵ���������Ӱ������ͼ��
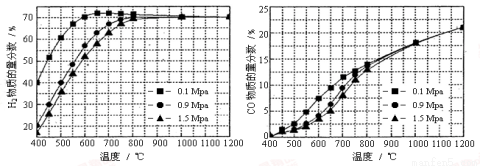
����Ҫ�ﵽH2���ʵ�������>65%��CO�����ʵ�������<10%����������������ʵ��� ��
A��600�棬0.9Mpa B��700�棬0.9Mpa C��800�棬1.5Mpa D��1000�棬1.5MPa
�ڻ���600�棬0��1Mpa�����£�ϵͳ��H2���ʵ��������淴Ӧʱ�䣨�ӳ��½��Ͽ�ʼ��ʱ���ı仯����ʾ��ͼ��
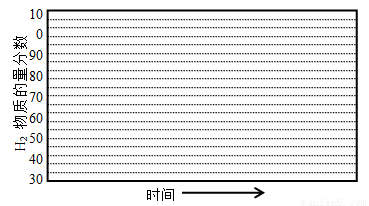
��6������������������������յ���H2���ʵ����������ͣ�ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ������ѧ�ڳ��ģ�����ۻ�ѧA���������棩 ���ͣ�ѡ����
�����£���10mL 0.1 mol��L-1��HR��Һ����ε���0.1 mol��L-1�İ�ˮ��������ҺpH�������Ա仯��ͼ�����з�������ȷ����
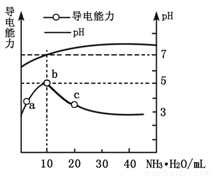
A��b����ҺpH=5����ʱ���ǡ���к�
B��a~b�㵼��������ǿ��˵��HRΪ����
C��c����Һ����c(NH4+)>c(R��)��c(OH��)>c(H+)
D��b~c�������Һ����c(H+)��c(OH��)=KW=1.0��10-14
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com