
| A. | 3.01×1023 | B. | 6.02×1023 | C. | 0.5 | D. | 1 |
科目:高中化学 来源: 题型:填空题
 目前工业合成氨的原理是:
目前工业合成氨的原理是:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+ Na+ Mn2+ S2- | B. | Na+ HCO3- Al3+ Cl- | ||
| C. | K+ Na+ Cl- S2- | D. | K+ Cl- Ba2+ OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
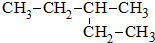
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | SO2通入溴水中 | 溶液褪色 | SO2有漂白性 |
| B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已氧化变质 |
| C | 向饱和碳酸钠溶液中通入CO2 | 有晶体析出 | 溶解度:NaHCO3>Na2CO3 |
| D | 向盛有少量NaHCO3的试管中滴加草酸溶液 | 有气泡产生 | 酸性:草酸>碳酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KC1 | B. | MgCl2 | C. | Na2CO3 | D. | K2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com