
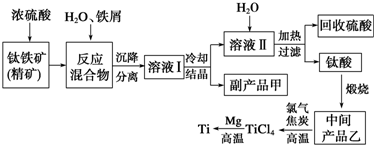
���� �������Ũ�����ϣ��������Ũ���ᷴӦ�IJ���֮һ��TiOSO4����Ӧ�����������ɣ�Ũ�������ǿ�����ԣ���+2��Fe���л�ԭ�ԣ���+2��Fe��Ũ������������Fe3+��Ȼ���������м���ˮ����м��������Ӧ2Fe3++Fe=3Fe2+���������ˣ���ҺI������ΪTiOSO4��FeSO4������Һ��ȴ�ᾧ�õ�����Ʒ����ҺII����������ͼ����ҺII�к���TiOSO4����Ʒ��Ϊ�̷�FeSO4•7H2O���Ƚ���ҺII�м���ˮ�����ȣ�TiO2+ˮ������H2TiO3��ˮ�����ӷ���ʽΪTiO2++2H2O$\frac{\underline{\;\;��\;\;}}{\;}$H2TiO3��+2H+��Ȼ����˻������ᣬͬʱ�õ�H2TiO3������H2TiO3��H2TiO3�ֽ�����TiO2��ˮ����Ӧ����ʽΪH2TiO3$\frac{\underline{\;\;��\;\;}}{\;}$TiO2+H2O�����ܺ�������C�ڸ����·���������ԭ��Ӧ����TiCl4��������TiO2����Ӧ����ʽΪTiO2+2Cl2+2C$\frac{\underline{\;����\;}}{\;}$TiCl4+2CO���ڸ��������£���Mg�����Ȼ��ѷ����û���Ӧ����Ti����Ӧ����ʽΪ2Mg+TiCl4$\frac{\underline{\;����\;}}{\;}$Ti+2MgCl2���ݴ˷������
��� �⣺�������Ũ�����ϣ��������Ũ���ᷴӦ�IJ���֮һ��TiOSO4����Ӧ�����������ɣ�Ũ�������ǿ�����ԣ�+2��Fe���л�ԭ�ԣ���+2��Fe��Ũ������������Fe3+��Ȼ���������м���ˮ����м��������Ӧ2Fe3++Fe=3Fe2+���������ˣ���ҺI������ΪTiOSO4��FeSO4������Һ��ȴ�ᾧ�õ�����Ʒ����ҺII����������ͼ����ҺII�к���TiOSO4����Ʒ��Ϊ�̷�FeSO4•7H2O���Ƚ���ҺII�м���ˮ�����ȣ�TiO2+ˮ������H2TiO3��ˮ�����ӷ���ʽΪTiO2++2H2O$\frac{\underline{\;\;��\;\;}}{\;}$H2TiO3��+2H+��Ȼ����˻������ᣬͬʱ�õ�H2TiO3������H2TiO3��H2TiO3�ֽ�����TiO2��ˮ����Ӧ����ʽΪH2TiO3$\frac{\underline{\;\;��\;\;}}{\;}$TiO2+H2O�����ܺ�������C�ڸ����·���������ԭ��Ӧ����TiCl4��������TiO2����Ӧ����ʽΪTiO2+2Cl2+2C$\frac{\underline{\;����\;}}{\;}$TiCl4+2CO���ڸ��������£���Mg�����Ȼ��ѷ����û���Ӧ����Ti����Ӧ����ʽΪ2Mg+TiCl4$\frac{\underline{\;����\;}}{\;}$Ti+2MgCl2��
��1��ͨ�����Ϸ���֪������Ʒ����FeSO4•7H2O�����FeSO4•7H2O�������������Σ�������KSCN��Һ���������ӣ�����鷽���ǣ�ȡ����Ʒ����������ˮ���μ�����KSCN��Һ���۲���Һ�Ƿ��ΪѪ��ɫ�������ΪѪ��ɫ��˵�����ʣ������ʣ�
�ʴ�Ϊ��ȡ����Ʒ����������ˮ���μ�����KSCN��Һ���۲���Һ�Ƿ��ΪѪ��ɫ�������ΪѪ��ɫ��˵�����ʣ������ʣ�
��2��������м��Ŀ���dz�ȥ�������ҷ�ֹ�������ӱ��������ʴ�Ϊ����ȥ�������ҷ�ֹ�������ӱ�������
��3��ͨ�����Ϸ���֪��TiO2+ˮ������H2TiO3�����ӷ���ʽΪTiO2++2H2O$\frac{\underline{\;\;��\;\;}}{\;}$H2TiO3��+2H+���ʴ�Ϊ��TiO2++2H2O$\frac{\underline{\;\;��\;\;}}{\;}$H2TiO3��+2H+��
��4��Ϊ��ֹ̼��������Ӧ��Ӧ�ɾ��������ȣ��ʴ�Ϊ������������
��5���������л�����������þ���������Ϣ֪�ѵĻ�ѧ���Ժ�С�������������ȼ���������Ӧ������������ӣ��ʴ�Ϊ��ϡ���
��6��������ҺI�Ƚ��м��Ⱥ���ȴ�ᾧ��TiOSO4����ˮ���������������̷��������̷������½�����ɽ����Ѳ����½���
�ʴ�Ϊ��TiOSO4����ˮ���������������̷��������̷������½�����ɽ����Ѳ����½���
��7��������Һֻ������ʽ�ζ���ʢ�ţ��Ȼ�����ǿ�������Σ�����Һ�����ԣ������Ȼ�����Һ����ʽ�ζ���ʢ�ţ�
�����Ӻ������ӷ����ķ�ӦΪ��Ti3+����ɫ��+Fe3++H2O=TiO2+����ɫ��+Fe2++2H+����Ϸ���ʽ3 TiO2++Al+6H+=3Ti3++Al3++3H2O��TiO2+��Fe3+�Ĺ�ϵʽΪTiO2+----Fe3+��
�������Һ��TiOSO4�����ʵ���Ũ����xmol/L��
TiO2+----Fe3+
1 1
��0.01x��$\frac{1}{5}$��mol ��0.1000��0.03��mol
1��1=��0.01x��$\frac{1}{5}$��mol����0.1000��0.03��mol
x=$\frac{��0.1000��0.03��mol��1}{��0.01��\frac{1}{5}��mol��1}$=1.5��
�ʴ�Ϊ����ʽ�ζ��ܣ�1.5mol/L��
���� ���⿼�����ʵ��Ʊ�ʵ�鷽����ƣ�Ϊ�߿���Ƶ�㣬���ؿ���ѧ����֪ʶ��Ӧ�á�����ʵ��������������������ȣ���ȷʵ��ԭ�������������淶���ǽⱾ��ؼ����ܴ������Ϸ������գ�֪��ÿһ�������ķ�Ӧ��������������Ŀ�Ѷ��еȣ�


 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ��${\;}_{88}^{226}$Raԭ���к���138������ | |
| B�� | RaԪ��λ��Ԫ�����ڱ��е������ڢ�A�� | |
| C�� | Ra���ܺ���ˮ��Ӧ�û����� | |
| D�� | Ra��OH��2��һ�������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ��������ϩ | B�� | һ�����м������ϩ | ||
| C�� | һ�����м��� | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | �缫���� | �������Һ | ������ָ��ƫת���� |
| 1 | Al��Mg | ϡ���� | ƫ��Al |
| 2 | Al��Cu | ϡ���� | ƫ��Cu |
| 3 | Al��ʯī | ϡ���� | ƫ��ʯī |
| 4 | Al��Mg | �������� | ƫ��Mg |
| 5 | Al��Zn | ϡ���� | ƫ��Al |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| t/min | 1 | 4 | 8 | 11 |
| n��H2��/mol | 6 | 2.6 | 2 | 2 |
| A�� | ���¶��£�ƽ�ⳣ��K=0.5 | |
| B�� | ��Ӧ����4minʱ��V��C02��=0.45 mol/��L•min�� | |
| C�� | ��Ӧ���е�9minʱ��H2��ת���ʱ�8minʱ�� | |
| D�� | ��Ӧ����11min��������������ѹǿ��CO2��ת����һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ش��� | X | Y | Z | W |
| ԭ�Ӱ뾶/pm | 160 | 143 | 70 | 66 |
| ��Ҫ���ϼ� | +2 | +3 | +5��+3��-3 | -2 |
| A�� | XԪ�صĵ��ʳ��������� | |
| B�� | һ�������£�Z������W�ij�������ֱ�ӻ����������������� | |
| C�� | Y������������Ӧ��ˮ����������ϡ��ˮ | |
| D�� | һ�������£�W���ʿ��Խ�Z���ʴ����⻯�����û����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 16��30��58��72 | B�� | 16��28��40��52 | C�� | 16��32��48��54 | D�� | 16��30��42��56 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com