
 ������M�����Ӿ۷�Ӧ����Ľṹ��ʽ
������M�����Ӿ۷�Ӧ����Ľṹ��ʽ ��
�� ���� ��1������������������������ܺͼ�Һ��Ӧ�����������Դ���̼�ᣬ�����ܺͿ�����̼���η�Ӧ��
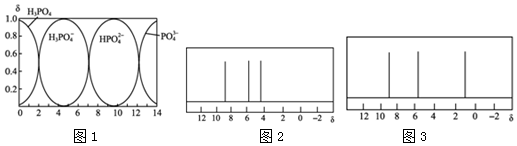
��2������Һ��H2PO4-Ũ�ȼ�С��H3PO4Ũ�����ݴ���д���ӷ���ʽ��
�ڸ�����Һ�д��ڵ���������ҺpH�Ĺ�ϵ�жϣ�
��3��3BrF3+5H2O�THBrO3+Br2+9HF+O2�У�BrԪ�ػ��ϼ���+3�۱�Ϊ+5�ۡ�-1�ۣ�����OԪ�ػ��ϼ���-2�۱�Ϊ0�ۣ�����Ӧ�в�����1.5mol O2������ת�Ƶ����غ���㱻ˮ��ԭ��BrF3�����ʵ�����
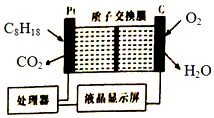
��4��C5H6�ĺ˴Ź���������3�����շ壬˵����������Hԭ�ӣ��÷��Ӳ����Ͷ�=$\frac{5��2+2-6}{2}$=3��˵����������̼̼˫�����ҷ��������ĸ����ʽṹ��ʽΪ ��C5H6��Br2 1��1�ӳɺ������M��N���֣�M�ĺ˴Ź���������3��Hԭ�ӣ����Ը�����Ϊ����1��4�ӳɺ�IJ���ݴ˷�����
��C5H6��Br2 1��1�ӳɺ������M��N���֣�M�ĺ˴Ź���������3��Hԭ�ӣ����Ը�����Ϊ����1��4�ӳɺ�IJ���ݴ˷�����
��� �⣺��1������������������������ܺͼ�Һ��Ӧ�����������Դ���̼�ᣬ�����ܺͿ�����̼���η�Ӧ������ϡ������ܵõ����������ҵõ����ʣ���ѡ��bd��
��2���ٸ���ͼ��֪��pH��5ת��Ϊ0ʱ����Һ��H2PO4-Ũ�ȼ�С��H3PO4Ũ���������ӷ�Ӧ����ʽΪH2PO4-+H+=H3PO4���ʴ�Ϊ��H2PO4-+H+=H3PO4��
�ڸ���ͼ֪��H2PO4-���ڵ�pH��ΧΪ0��10��PO43-���ڵ�pH��10�����Զ��߲��ܹ��棬�ʴ�Ϊ�����ܣ�
��3��3BrF3+5H2O�THBrO3+Br2+9HF+O2�У�BrԪ�ػ��ϼ���+3�۱�Ϊ+5�ۡ�-1�ۣ�����OԪ�ػ��ϼ���-2�۱�Ϊ0�ۣ�����Ӧ�в�����1.5mol O2����ʧȥ���ӵ����ʵ���=1.5mol��4=6mol������ת�Ƶ����غ�ñ�ˮ��ԭ��BrF3�����ʵ���=$\frac{6mol}{3-0}$=2mol��
�ʴ�Ϊ��2��
��4��C5H6�ĺ˴Ź���������3�����շ壬˵����������Hԭ�ӣ��÷��Ӳ����Ͷ�=$\frac{5��2+2-6}{2}$=3��˵����������̼̼˫�����ҷ��������ĸ����ʽṹ��ʽΪ ��C5H6��Br2 1��1�ӳɺ������M��N���֣�M�ĺ˴Ź���������3��Hԭ�ӣ����Ը�����Ϊ����1��4�ӳɺ�IJ�������M�����Ӿ۷�Ӧ����Ľṹ��ʽΪ
��C5H6��Br2 1��1�ӳɺ������M��N���֣�M�ĺ˴Ź���������3��Hԭ�ӣ����Ը�����Ϊ����1��4�ӳɺ�IJ�������M�����Ӿ۷�Ӧ����Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�� ��
��
���� ���⿼����ۺϣ��漰����������pH�Ĺ�ϵ��������ԭ��Ӧ�ļ��㡢��˹���ɵ�֪ʶ�㣬ͬʱ����ѧ������ͼ��������������ѵ��ǣ�3������㣬ע��ˮ��BrF3��Ԫ�ػ��ϼ۱仯��Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�м�������NaHCO3���� | B�� | ��ˮ�е�������ϡ���� | ||
| C�� | ��ˮ�м��������Ȼ������� | D�� | ��ˮ���ȵ�100�棬���pH=6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯī�缫��������������ԭ��Ӧ | |
| B�� | ���缫�ĵ缫��Ӧʽ��C8H18+16H2O-50e-�T8CO2��+50H+ | |
| C�� | H+�����ӽ���Ĥ������Ҳ�Ǩ�� | |
| D�� | ÿ����5.6LO2����·��ͨ��1 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 п-������أ�ԭ����ͼ�������������е綯���Ķ�����Դ���õ�طŵ�ʱZnת��ΪZnO���õ�ع���ʱ����˵����ȷ���ǣ�������
п-������أ�ԭ����ͼ�������������е綯���Ķ�����Դ���õ�طŵ�ʱZnת��ΪZnO���õ�ع���ʱ����˵����ȷ���ǣ�������| A�� | ������ʯī�缫�Ϸ���������Ӧ | |
| B�� | �õ�صĸ�����ӦΪZn+H2O-2e-=ZnO+2H+ | |
| C�� | �õ�طŵ�ʱOH-��ʯī�缫�ƶ� | |
| D�� | �õ�س��ʱӦ��Zn�缫���Դ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ǧ�����ڳ������У������������������� | |
| B�� | ��״���£�22.4 L CCl4��CH2O�Ļ�����к���6.02��1023��̼ԭ�� | |
| C�� | 0.1 mol•L-1 CH3COOH��Һ��ˮϡ�ͣ���Һ�е�����Ũ�Ⱦ���С | |
| D�� | ��CH3COONa��Һ��20��������30�棬��Һ�д��������Ũ�ȼ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1mol/LFeC13��Һ�У�A13+��NH4+��Cl-��SCN- | |
| B�� | ʹ���ȱ��ɫ����Һ�У�Mg2+��K+��SO42-��NO3- | |
| C�� | $\frac{{K}_{W}}{c��{H}^{+}��}$=1��10-15mol/L����Һ�У�Na+��Fe3+��I-��AlO2- | |
| D�� | ˮ�����c��H+��=1��10-13mol/L����Һ�У�K+��Na+��CO32-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ֻ���ᡢ��������ʲ����ڵ���� | |
| B�� | �Ȼ�����Һ�ڵ��������µ���Ϊ�������������� | |
| C�� | �����δ���ܵ��磬�ܵ����Ҳδ���ǵ���� | |
| D�� | ���ᱵ��ˮ��Һ�䵼���Լ����������ᱵ��ǿ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
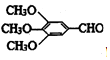 ���Ϳ����ҩ��H��
���Ϳ����ҩ��H��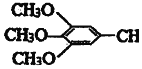 =CHCONHCH��CH3��2����·����ͼ�����ַ�Ӧ��ȥ�������Լ�����
=CHCONHCH��CH3��2����·����ͼ�����ַ�Ӧ��ȥ�������Լ�����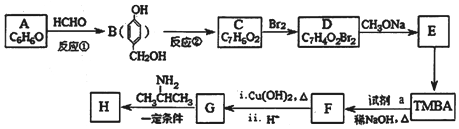
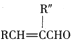 ��R��R���ʾ�������⣩
��R��R���ʾ�������⣩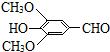 ���Լ�a�ķ���ʽ��C2H4O��
���Լ�a�ķ���ʽ��C2H4O��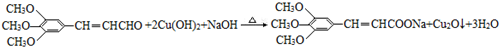 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 Na2S2O3����Ҫ�Ļ���ԭ�ϣ�������ˮ�������Ի���Ի������ȶ���
Na2S2O3����Ҫ�Ļ���ԭ�ϣ�������ˮ�������Ի���Ի������ȶ����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com