
根据离子方程式[ ]+XO3-+6H+=3X2+3H2O判断,下列说法正确的是
A.X2的电子式为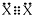 B.X位于元素周期表中第VA族
B.X位于元素周期表中第VA族
C.X元素原子的最外层有7个电子 D.X可能位于元素周期表中第二周期
科目:高中化学 来源:2016-2017学年山西省高二上开学考化学试卷(解析版) 题型:选择题
分析推理是化学学习的方法之一。下列实验推理中,正确的是
A.金属的冶炼方法与金属的活泼性有很大关系,所以银和汞可以用热分解的方法冶炼
B.钠比铜活泼,所以钠可以从硫酸铜溶液中置换出铜
C.工业上电解熔融氯化镁可制得金属镁,所以工业上电解熔融氯化铝可制得铝
D.将镁条和铝片用导线连接后插进稀NaOH溶液,镁条上产生气泡,说明镁比铝活泼
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期周考(8.28)化学试卷(解析版) 题型:填空题
(1)己知Fe(OH)3能与次氯酸盐发生如下反应(未配平): Fe(OH)3+ClO-+OH-→FeO4n-+Cl-+H2O
(1)已知有10.7g Fe(OH)3参加反应,共转移了0.3NA个电子,则n=______,FeO4n- 中铁元素的化合价为______.
(2)根据所学的知识,推测FeO4n-能和下列______(填序号)物质反应.
A、KMnO4 B、SO2 C、H2S D、O2.
(2)一定条件下,向含硝酸的废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32gCH3OH,转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是_________。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期周考(8.28)化学试卷(解析版) 题型:选择题
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。下列各组物质中由于浓度不同而能发生不同氧化还原反应的是( )
① Cu与HNO3溶液;② Fe与HCl溶液;③Zn与H2SO4溶液;④铝与NaOH溶液
A.①③ B.①② C.②④ D.②③
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上学期开学考试化学试卷(解析版) 题型:实验题
苯甲酸(无色针状晶体,熔点122.4℃)可广泛用于医药、染料载体、香料等,实验室用甲苯和高锰酸钾制备苯甲酸。反应方程式如下:
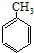 +2KMnO4
+2KMnO4
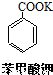 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
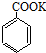 +HCl→
+HCl→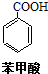 +KCl
+KCl

已知有关化合物的相关数据如表所示:
化合物 | 相对分子质量 | 密度(g/cm3) | 溶解性 | 沸点(℃) |
甲苯 | 92 | 0.87 | 难溶于水 | 110.0 |
苯甲酸钾 | 160 | — | 易溶于水 | — |
苯甲酸 | 122 | 1.26 | 微溶于水 | 248.0 |
苯甲酸在100g水中的溶解度0.18g(4℃),0.27g(18℃),2.2g(75℃)。
合成:如上图(固定及加热装置略去)所示,在三颈烧瓶中加入4.23mL甲苯和100mL蒸馏水,瓶口装上温度计、电动搅拌器、冷凝管,慢慢开启电动搅拌器,加热至沸腾。经冷凝管上口分批加入21.30g高锰酸钾(过量),继续煮沸至甲苯层消失,回流液中不再出现油珠为止,得到反应混合物。
对反应混合物进行分离:①趁热过滤→②洗涤滤渣→③合并滤液和洗涤液→④冷却→⑤盐酸酸化→⑥过滤。
对粗产品苯甲酸进行提纯:①沸水溶解→②活性炭脱色→③趁热过滤→④_________→⑤过滤→⑥洗涤→⑦干燥。
请回答下列问题:
(1)实验室中量取4.23mL甲苯所需仪器为_________。
(2)冷凝管的上口是否需要塞上塞子________(填“是”或“否”),a处水流方向是_______(填“进水”或“出水”)。
(3)高锰酸钾需要分批加入,请用化学反应速率观点说明理由_________。
(4)在对粗产品苯甲酸进行提纯过程中,“③趁热过滤”的目的是_________;“④”的操作名称是________;可证明“⑥洗涤”步骤已洗涤干净的方法是_____________。
(5)干燥后称量得苯甲酸2.93g,则苯甲酸的产率为________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上入学考试化学试卷(解析版) 题型:简答题
(1)现有 CH4、C2H4、C3H4、C2H6、C3H6 五种有机物。同质量的以上物质完全燃烧时消耗 O2的量最多的是 ;同状况、同体积的以上五种物质完全燃烧时消耗 O2的量最多的是 ;同质量的以上五种物质燃烧时,生成 CO2 的量最多的 , 生成 H2O的量最多的是 。
(2)以乙烯和水为主要原料选取其他必要的无机物制取乙酸乙酯,写出对应的化学方程式
已知:乙醛可氧化为乙酸(该方程式不用写)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上入学考试化学试卷(解析版) 题型:选择题
某有机物的结构如图所示,这种有机物不可能具有的性质是
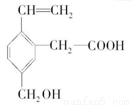
①可以燃烧;②能使酸性 KMnO4 溶液退色;③能跟 NaOH 溶液反应;
④能发生酯化 反应;⑤能发生加成反应;⑥能发生水解反应
A.①④ B.只有⑥ C.只有⑤ D.④⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一上入学考试化学卷(解析版) 题型:选择题
只用一种物质一次就能将稀硫酸、水、澄清石灰水三种无色液体鉴别出来,可供选用的物质是:①PH试纸 ②酚酞试液 ③稀盐酸 ④碳酸钠溶液 ⑤石蕊试液,其中能用于鉴别的是
A.①④⑤ B、①②⑤ C、①②③ D、③④⑤
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三第一次月考理综化学试卷(解析版) 题型:实验题
【化学──选修2:化学与技术】
利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
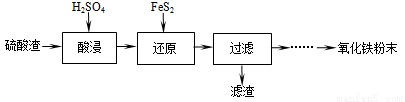
(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率,② 。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42-,该反应的离子方程式为 。
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。实验步骤为:
准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++SnCl62-,
Sn2++4Cl-+2HgCl2=SnCl62-+Hg2Cl2↓,
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O。
①若SnCl2不足量,则测定的Fe3+量 (填“偏高”、“偏低”、“不变”,下同)。
②若不加HgCl2,则测定的Fe3+量 。
(4)①可选用 (填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是 (用离子反应方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:

实验可选用的试剂有:稀HNO3、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a. 氧化: ;
b. 沉淀: ;
c. 分离,洗涤;
d. 烘干,研磨。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com