
| A. | 1molCH3+所含的电子数为9NA | |
| B. | 标准状况下,11.2 L HF的分子数为0.5NA | |
| C. | 39 g Na2O2与足量水反应,转移电子数为NA | |
| D. | 1 mol乙醇中含有共用电子对数为8NA |
分析 A.CH3+中含8个电子;
B.标况下,HF为液体;
C.Na2O2与足量水反应,过氧化钠既是氧化剂又是还原剂,所以1mol Na2O2与足量水反应转移的电子的物质的量为1mol;
D.1个C2H6O中含8对共用电子对来计算.
解答 解:A.1molCH3+所含的电子数为8NA,故A错误;
B.标况下,HF为液体,不能使用气体摩尔体积,故B错误;
C.39 g Na2O2物质的量为$\frac{39g}{78g/mol}$=0.5mol,与足量水反应,转移电子数为0.5NA,故C错误;
D.1个C2H6O中含8对共用电子对,所以1 mol乙醇中含有共用电子对数为8NA,故D正确;
故选:D.
点评 本题考查阿伏伽德罗常数的使用及有关计算,难度不大,注意气体摩尔体积的使用范围和条件,注意乙醇分子的构成是解题关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发现了电子 | B. | 根据α提出了带核的原子结构模型 | ||
| C. | 引入的量子学说 | D. | 提出较为系统的化学原子学说 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
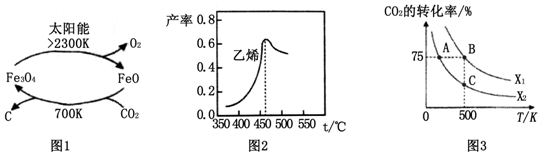
| 时间/min 浓度/mol•L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
| H2(g) | 6.00 | 5.40 | 5.10 | 9.00 | 8.40 | 8.40 |
| CO2(g) | 2.00 | 1.80 | 1.70 | 3.00 | 2.80 | 2.80 |
| CH2=CH2(g) | 0 | 0.10 | 0.15 | 0.50 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3$→_{催化剂}^{O_{2}}$NO$\stackrel{NaOH溶液}{→}$NaNO3 | |
| B. | Fe2O3$→_{高温}^{Al}$Fe$→_{点燃}^{Cl_{2}}$FeCl3 | |
| C. | SiO2$→_{△}^{H_{2}O}$H2SiO3$\stackrel{NaOH溶液}{→}$NaSiO3 | |
| D. | NaSO4溶液$\stackrel{BaCl_{2}溶液}{→}$BaSO4$\stackrel{盐酸}{→}$BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2L 1mol/L过氧化氢溶液中含氧原子数为4NA | |
| B. | 6.8g熔融的KHSO4中含有0.1NA个阳离子 | |
| C. | 2mol MnO2与足量的浓盐酸加热充分反应,转移电子数为4NA | |
| D. | 密闭容器中2molNO2和1molO2充分反应,产物分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自来水 | B. | 0.5mol/L的盐酸 | ||
| C. | 0.5mol/L的醋酸 | D. | 0.5mol/L的氯化钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
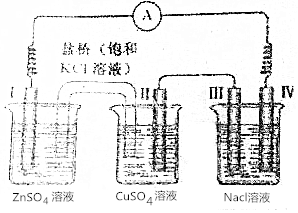
| A. | 电子由电极Ⅳ通过外电路流向电极Ⅰ | |
| B. | 装置工作过程中Ⅲ电极周围出现红色 | |
| C. | 电极Ⅱ发生还原反应 | |
| D. | 盐桥中Cl-向乙池移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com