
| A£® | 0.1 mol | B£® | 0.2 mol | C£® | 0.3 | D£® | 0.4 mol |
·ÖĪö øł¾Żµē½ā³ŲµÄ¹¤×÷ŌĄķ£¬ŅŖĻėČƵē½āŗóµÄµē½āÖŹø“Ō£¬Ōņ×ńѵÄŌŌņŹĒ£ŗ³öŹ²Ć“¼ÓŹ²Ć“£¬¼ÓČė Cu£ØOH£©2ŗóČÜŅŗÓėµē½āĒ°ĻąĶ¬£¬ŌņĶĄė×ÓŗĶĒāŃõøł·Åµē£®
½ā“š ½ā£ŗŅŌ¶čŠŌµē¼«µē½āCuSO4ČÜŅŗµÄµē½āŌĄķ·½³ĢŹ½ŹĒ£ŗ2Cu2++2H2O$\frac{\underline{\;µē½ā\;}}{\;}$2Cu+4H++O2”ü£¬¼ÓČė0.1molCu£ØOH£©2£ØĻąµ±ÓŚCuOŗĶH2O£©ŗóČÜŅŗÓėµē½āĒ°ĻąĶ¬£¬øł¾ŻĶŌŖĖŲŹŲŗć£¬ĖłŅŌĪö³ö½šŹōĶµÄĪļÖŹµÄĮæŹĒ0.1mol£¬Ņõ¼«·“Ó¦ŹĒ£ŗ2Cu2++4e-”ś2Cu£¬µ±Īö³ö½šŹōĶµÄĪļÖŹµÄĮæŹĒ0.1molŹ±£¬Ōņ×ŖŅʵĵē×ÓŹĒ0.2mol£¬µ±µē½āµō0.1molĖ®Ź±£¬×ŖŅʵē×ÓŹĒ0.2mol£¬×ܹ²×ŖŅʵē×ÓŹĒ0.4mol£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éѧɜµē½ā³ŲµÄ¹¤×÷ŌĄķ£¬×¢Ņāµē×ÓŹŲŗćĖ¼ĻėµÄÓ¦ÓĆ£¬æÉŅŌøł¾ŻĖłŃ§ÖŖŹ¶½ųŠŠ»Ų“š£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| X | Y | |
| Z | W |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·²ŹĒĪüČČ·“Ó¦¶¼ŠčŅŖ¼ÓČČ | |
| B£® | ĪļÖŹµÄ»Æѧ±ä»Æ¶¼°éĖę×ÅÄÜĮæ±ä»Æ | |
| C£® | ±ķŹ¾ÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½£ŗNaOH+HClØTNaCl+H2O”÷H=-57.3 kJ•mol-1 | |
| D£® | µČÖŹĮæµÄĮņÕōĘųŗĶĮņ¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬Ē°Õߵķ“Ó¦ČȱČŗóÕß“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | b-a-4 | B£® | b-a-8 | C£® | b+a+8 | D£® | b-a-12 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ×å ÖÜĘŚ | I A | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | J | F | H |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
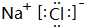 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
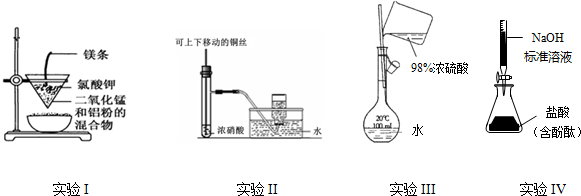
| A£® | ŹµŃéI£ŗÖʱø½šŹōĆĢ | |
| B£® | ŹµŃéII£ŗÖʱø²¢ŹÕ¼ÆNO2 | |
| C£® | ŹµŃéIII£ŗÅäÖĆŅ»¶ØµÄĪļÖŹµÄĮæÅØ¶ČµÄĻ”ĮņĖįČÜŅŗ | |
| D£® | ŹµŃéIV£ŗ²ā¶ØĪ“ÖŖŃĪĖįµÄÅØ¶Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
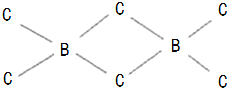
£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com