
 ,实验中,可以观察到反应②的现象是:无色气体变为红棕色.
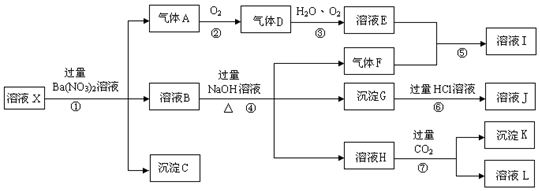
,实验中,可以观察到反应②的现象是:无色气体变为红棕色.分析 某强酸性溶液X,则溶液中不存在弱酸根离子CO32-、SiO32-,溶液和硝酸钡溶液反应生成沉淀C,则溶液存在SO42-,不存在和硫酸根离子反应的Ba2+,C是BaSO4;酸性条件下硝酸根离子具有强氧化性,所以溶液中Fe2+和NO3-不能共存,加入硝酸钡产生气体,则溶液中存在Fe2+,不存在NO3-,气体A是NO,由反应②可知生成D为NO2,③中生成E为硝酸;溶液B中加入过量氢氧化钠溶液时,产生气体F,则溶液中含有NH4+,F是NH3,产生沉淀,由于溶液中存在Fe2+,沉淀G是Fe(OH)3,溶液H中通入过量二氧化碳生成沉淀,则溶液中存在Al3+,溶液H中含有偏铝酸根,沉淀K是Al(OH)3,溶液L是NaHCO3,以此来解答.
解答 解:(1)产生气体A的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO+2H2O,故答案为:3Fe2++NO3-+4H+=3Fe3++NO+2H2O;
(2)F是NH3,电子式为 ,气体A是NO,为无色气体,与氧气反应生成红棕色的NO2,故答案为:
,气体A是NO,为无色气体,与氧气反应生成红棕色的NO2,故答案为: ;无色气体变为红棕色;
;无色气体变为红棕色;
(3)溶液Ⅰ中的含有的阳离子是铵根离子,铵根离子的检验方法是:取样,加碱(NaOH)溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,
故答案为:取样,加碱(NaOH)溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体;
(4)由以上分析可知沉淀G是Fe(OH)3,溶液H中含有偏铝酸根,通入二氧化碳生成沉淀K是Al(OH)3,方程式为NaAlO2+2H2O+CO2═Al(OH)3↓+NaHCO3,故答案为:Fe(OH)3;NaAlO2+2H2O+CO2═Al(OH)3↓+NaHCO3;
(5)由以上分析可知肯定存在的离子为Fe2+、Al3+、NH4+、SO42-,可能存在的离子为Fe3+,故答案为:Fe2+、Al3+、NH4+、SO42-;Fe3+.
点评 本题考查无机物的推断,为高频考点,把握离子的性质、发生的反应为解答的关键,侧重分析与实验能力的考查,注意发生的氧化还原反应,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 天然油脂的主要成分是高级脂肪酸 | |
| B. | 分馏、干馏都是物理变化,裂化、裂解都是化学变化 | |
| C. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 | |
| D. | 乙酸与乙醇可以发生酯化反应,又均可与金属钠发生置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
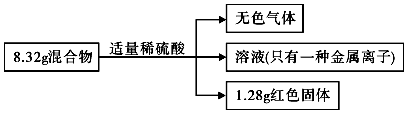
| A. | 无色气体的体积为2.24L | |
| B. | 原混合物中铁的质量为6.72g | |
| C. | 反应后的溶液中金属离子物质的量为0.02 mol | |
| D. | 反应消耗的H2SO4物质的量为0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2、NaHSO4 | B. | Na2CO3、HNO3 | C. | NaHCO3、AlCl3 | D. | NaOH、CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
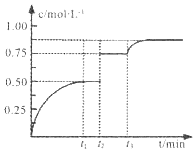 一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )
一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )| A. | 反应方程式中的x=1 | |
| B. | t2时刻改变的条件是使用催化剂 | |
| C. | t3时刻改变的条件是移去少量物质C | |
| D. | t1~t3间该反应的平衡常数均为4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业制金属钠:电解饱和食盐水 | |
| B. | 工业炼铁:需要用到的原料有铁矿石、一氧化碳、空气和石灰石 | |
| C. | 冶炼镁:将六水合氯化镁晶体在一定条件下加热得到无水氯化镁,电解熔融氯化镁,可以得到金属镁 | |
| D. | 生物炼铜法:利用某种能耐受铜盐毒性的细菌,这种细菌利用空气中的填氧气氧化硫化铜矿石,把不溶性的硫化铜直接转化为单质铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 0.2mol/L的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) | |
| C. | 0.1mol/L的NH4Cl溶液与0.05mol/L的NaOH溶液等体积混合,其混合溶液中:c(Cl-)>c(NH4+)>c(Na+)>c(H+)>c(OH-) | |
| D. | c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液中:c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{3}^{4}$He | B. | ${\;}_{2}^{3}$He | C. | ${\;}_{2}^{4}$He | D. | He${\;}_{3}^{3}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com