
磷在氧气中燃烧,可能生成两种固态氧化物。3.1 g的单质磷(P)在3.2 g氧气中燃烧,至反应物耗尽,并放出X kJ热量。
(1)通过计算确定反应产物的组成(用化学式表示)是 ,其相应的质量(g)为 。
(2)已知单质磷的燃 烧热为Y kJ/mol,则1mol P与O2反应生成固态P2O3的反应热ΔH= 。
烧热为Y kJ/mol,则1mol P与O2反应生成固态P2O3的反应热ΔH= 。
(3)写出1mol P与O2反应生成固态P2O3的热化学方程式: 。
【答案】
(1)P2O3 P2O5 2.75 3.55
(2)-(20X-Y)kJ/mol
(3)P(s)+ O2(g)=
O2(g)= P2O2(s);
P2O2(s); △H=-(20X-Y)kJ/mol
△H=-(20X-Y)kJ/mol
【解析】3.1 g P在3.2 g O2中充分燃烧后,产物中n(P)∶n(O)=1∶2,可知其中必然有P2O5,另一种固态氧化物为P2O3。列出方程组:

解得:n(P2O5)=0.025 mol,n(P2O3)=0.025 mol,质量分别为3.55 g和2.75 g。
P的燃烧热是1 mol P充分燃烧生成P2O5时放出的热量,则1 mol P与O2反应生成固态P2O3时放出的热量为: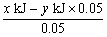 =(20x-y) kJ,即反应热ΔH=-(20x-y)kJ·mol-1。
=(20x-y) kJ,即反应热ΔH=-(20x-y)kJ·mol-1。
热化学方程式为:P(s)+ O2(g)====
O2(g)==== P2O3(s);ΔH=-(20x-y)kJ·mol-1
P2O3(s);ΔH=-(20x-y)kJ·mol-1


科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.标况下,11.2L SO3所含的分子数目为0.5 NA
B.室温下,1L pH=1的稀硫酸溶液中,由水电离的H+离子数目为0.2NA
C.铅蓄电池放电时,正极消耗4mol H+,则电路中通过的电子数目为2NA
D.8 Al + 3 NH4ClO4 == 4 Al2O3 +3NH3 +3HCl 反应中,消耗27gAl粉时,转移的电子数目为2.75NA(Al原子量—27)
查看答案和解析>>
科目:高中化学 来源: 题型:
磷单质及其化合物有广泛应用。
(1)由磷灰石[主要成分Ca5(PO4)3F]在高温下制备黄磷(P4)的热化学方程式为:4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) ΔH
①上述反应中,副产物矿渣可用来___________________________________。
②已知相同条件下:
4Ca5(PO4)3F(s)+3SiO2(s)====6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) ΔH1
2Ca3(PO4)2(s)+10C(s)====P4(g)+6CaO(s)+10CO(g) ΔH2
SiO2(s)+CaO(s)====CaSiO3(s) ΔH3
用ΔH1、ΔH2和ΔH3表示ΔH,ΔH=_____________________________。
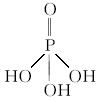
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式见下图)之间脱去两个水分子的产物,其结构式为________________________。三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为___________________________。
(3)次磷酸钠(NaH2PO2)可用于化学镀镍。
①NaH2PO2中P元素的化合价为________________________。
②化学镀镍的溶液中含有Ni2+和 ,在酸性等条件下发生下述反应:
,在酸性等条件下发生下述反应:
(a)__________Ni2++______ ____
____ +__________
+__________ __________Ni+________
__________Ni+________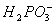 +_______
+_______
(b)6 +2H+====2P+4
+2H+====2P+4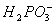 +3H2↑
+3H2↑
请在答题卡上写出并配平反应式(a)。
③利 用②中反应可在塑料镀件表面沉积镍磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀。请从以下方面比较化学镀与电镀。
用②中反应可在塑料镀件表面沉积镍磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀。请从以下方面比较化学镀与电镀。
方法上的不同点:_______________;原理上的相同点:_______________;化学镀的优点:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是
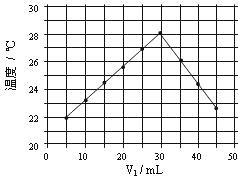
A 做该实验时环境温度为22℃
B 该实验表明化学能可能转化为热能
C NaOH溶液的浓度约为1.0mol/L
D 该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O2(g)==CO2(g);△H1 C(s)+ O2(g)==CO(g);△H2
O2(g)==CO(g);△H2
②S(s)+O2(g)==SO2(g);△H3 S(g)+O2(g)==SO2(g);△H4
③H2(g)+ O2(g)==H2O(l);△H5 2H2(g)+O2(g)==2H2O(l);△H6
O2(g)==H2O(l);△H5 2H2(g)+O2(g)==2H2O(l);△H6
④CaCO3(s)==CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)==Ca(OH)2(s);△H8
A.① B.④ C.②③④ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的性质与氢键无关的是( )
A.冰的密度比液态水的密度小 B.NH3易液化
C.NH3 分子比PH3 分子稳定 D.在相同条件下,H2O的沸点比H2S的沸点高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列微粒中,未成对电子数最多的是( )
A.O:1s22s22p4 B.P:1s22s22p63s23p3
C.Mn:1s22s22p63s23p63d54s2 D.Cr:1s22s22p63s23p63d54s1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
A. X与Y组成化合物时,X显负价,Y显正价
B. 第一电离能Y一定小于X
C. 最高价含氧酸的酸性:X对应的酸性强于Y对应的酸性
D. 气态氢化物的稳定性:HmY小于HmX
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
A.H2SO4 的摩尔质量是 98 g B.1 mol H2O 的质量是 18 g/mol
C.Cl-的摩尔质量是 35.5 g/mol D.1 mol N2 的体积是 22.4 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com